题目内容
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、在1L 0.1mol/L的NH4NO3溶液中含氮原子数目为0.2NA |
| B、标准状况下22.4 L CH3CH2OH中碳原子数为2NA |
| C、0.2 mol?L-1 NaHCO3溶液中含Na+数为0.2NA |
| D、标准状况下,22.4L Cl2与足量的铁粉完全反应转移电子数目为3NA |
考点:阿伏加德罗常数
专题:
分析:A.1L0.1mol/L的NH4NO3溶液中含有溶质硝酸铵0.1mol,0.1mol硝酸铵中含有0.2mol氮原子;
B.气体摩尔体积只适用于气体;
C.溶液的体积未知;
D.标准状况下,22.4L氯气的物质的量为1mol,1mol氯气完全反应得到2mol电子.
B.气体摩尔体积只适用于气体;
C.溶液的体积未知;
D.标准状况下,22.4L氯气的物质的量为1mol,1mol氯气完全反应得到2mol电子.
解答:
解:A.1L0.1mol/L的NH4NO3溶液中含有溶质硝酸铵的物质的量为0.1mol,0.1mol硝酸铵中含有0.2mol氮原子,含有的氮原子数为0.2NA,故A正确;
B.标况下乙醇为液体,不能使用气体摩尔体积,故B错误;
C.溶液的体积未知,无法计算钠离子的物质的量,故C错误;
D.标况下22.4L氯气的物质的量为1mol,1mol氯气与足量铁完全反应生成2mol氯离子,转移了2mol电子,转移电子数目为2NA,故D错误;
故选:A.
B.标况下乙醇为液体,不能使用气体摩尔体积,故B错误;
C.溶液的体积未知,无法计算钠离子的物质的量,故C错误;
D.标况下22.4L氯气的物质的量为1mol,1mol氯气与足量铁完全反应生成2mol氯离子,转移了2mol电子,转移电子数目为2NA,故D错误;
故选:A.
点评:本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意明确标况下气体摩尔就他的使用条件.

练习册系列答案
相关题目
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A、Na+、K+、SiO32-、Cl- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、Na+、SO42-、Cl- |
| D、Ba2+、HCO3-、ClO-、K+ |
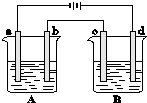 如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )
如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )| A、1:1:2:1 |
| B、2:1:1:1 |
| C、2:2:4:1 |
| D、2:1:2:1 |
下列现象或应用中,不能用胶体知识解释的是( )
| A、清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱 |
| B、用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
| C、在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
| D、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
下列说法正确的是( )
| A、CO2的相对分子质量为44g/mol |
| B、“物质的量”是“物质的质量”的简称 |
| C、摩尔只能用于计量纯净物 |
| D、阿伏伽德罗常数的单位是mol-1 |
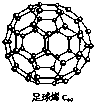 能源材料是当今科学研究的热点.氢气作为一种清洁能源,必须解决它的储存问题. C60(结构见图)可用作储氢材料.继C60后,科学家又合成了Si60、N60,它们的结构相似.下列有关说法正确的是( )
能源材料是当今科学研究的热点.氢气作为一种清洁能源,必须解决它的储存问题. C60(结构见图)可用作储氢材料.继C60后,科学家又合成了Si60、N60,它们的结构相似.下列有关说法正确的是( )| A、C60、Si60、N60都属于新型化合物 |
| B、C60、Si60、N60互为同分异构体 |
| C、N60结构中只存在N-N单键,而C60结构中既有C-C单键又有C=C双键 |
| D、已知金刚石中C-C键长154pm,C60中C-C键长140~145pm,故C60熔点高于金刚石 |