��Ŀ����
12��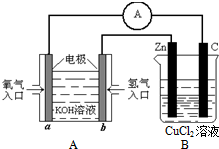 ��ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ��
��ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ����1����ѧ��Ӧ�зų������ܣ���H���뷴Ӧ���������ļ��ܣ�E���йأ�
��֪��H2��g��+Cl2��g��=2HCl��g����H=-185kJ/mol
E��H-H��=436kJ/mol��E��Cl-Cl��=247kJ/mol
��E��H-Cl��=434kJ/mol
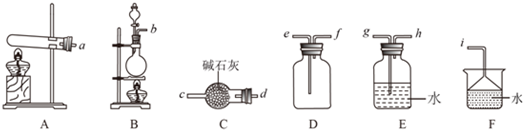
��2������ͼ��ʾ��װ�ã�
C��ʯī����Ϊ�������缫��ӦΪ2Cl--2e-=Cl2��ͨ��H2�⼫Ϊ��������a�������ĵ�O2�ڱ�״���µ����Ϊ2.24Lʱ��Zn�������仯Ϊ12.8gB�ز����������Ϊ4.48L����״����
��3�������й�����ȼ�ϵ�ص�������ȷ����CD
A���˵���ܷ�����ɫ����
B��������ӦΪH2-2e-+2OH-=2H2O
C������ʱ���������Һ��PH���ϼ�С
D������ȼ�ϵ����һ�ֲ���Ҫ����ԭ����������ȫ�������ڵ���ڵķ���װ�ã�
���� ��1����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ��ݴ˼��㣻
��2��B���ǵ��أ�C��ʯī����Ϊ�������缫��ӦʽΪ��2Cl--2e-=Cl2����ͨ��H2�⼫Ϊԭ��صĸ�������a�������ĵ�O2�ڱ�״���µ����Ϊ2.24Lʱ��������·ת�Ƶ��ӵ����ʵ���$\frac{2.24L}{22.4L/mol}$��4=0.4mol��Zn���ĵ缫��ӦʽΪ��Cu2++2e-=Cu����������ͭ�����ʵ���Ϊ��0.2mol������Ϊ��0.2mol��64g/mol=12.8g���������������ʵ���Ϊ��0.2mol���ɴ˷������
��3����ȼ�ϵ���ǽ���ѧ��ת��Ϊ���ܣ������ϵ缫��ӦʽΪ2H2+4OH--4e-=4H2O��������ӦʽΪO2+2H2O+4e-=4OH-����ط�ӦʽΪ2H2+O2=2H2O�������Һ��KOH�Ƿ�Ũ�ȱ仯�������
��� �⣺��1��436kJ/mol+247kJ/mol-2E��H-Cl��=-185kJ/mol�����E��H-Cl��=434KJ/mol���ʴ�Ϊ��434��
��2��B���ǵ��أ�C��ʯī����Ϊ�������缫��ӦʽΪ��2Cl--2e-=Cl2����ͨ��H2�⼫Ϊԭ��صĸ�������a�������ĵ�O2�ڱ�״���µ����Ϊ2.24Lʱ��������·ת�Ƶ��ӵ����ʵ���$\frac{2.24L}{22.4L/mol}$��4=0.4mol��Zn���ĵ缫��ӦʽΪ��Cu2++2e-=Cu����������ͭ�����ʵ���Ϊ��0.2mol������Ϊ��0.2mol��64g/mol=12.8g���������������ʵ���Ϊ��0.2mol���������������Ϊ��0.2mol��22.4L/mol=4.48L���ʴ�Ϊ��������2Cl--2e-=Cl2��������12.8g��4.48L��
��3��A���õ����ȼ�ϲ�ȼ�գ���ֱ�ӽ���ѧ��ת��Ϊ���ܣ����Բ��ܷ�����ɫ���棬��A����
B��ͨ�������ĵ缫Ϊ������ͨ�������ĵ缫Ϊ������������ӦʽΪO2+2H2O+4e-=4OH-����B����
C���ŵ�ʱ��Ӧ����������ˮ������KOHŨ�ȱ�С������Һ��pH��С����C��ȷ��
D������ȼ�ϵ����һ�ֲ���Ҫ����ԭ����������ȫ�������ڵ���ڵķ���װ�ã���D��ȷ��
��ѡCD��
���� ���⿼��ȼ�ϵ�أ���ȷ�������Ϸ����ķ�Ӧ�ǽⱾ��ؼ�������ȷ��д�缫��Ӧʽ��Ҫ��ϵ������Һ�������д���״�ѡ����C��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | �ڳ��³�ѹ�£�1mol��������ԭ����Ϊ2NA | |
| B�� | 0.5molO2��0.5molO3�Ļ���������е���ԭ�Ӹ���Ϊ2.5NA | |
| C�� | ���³�ѹ�£�2.24 LCO��CO2��������к��е�̼ԭ����ĿΪ0.1NA | |
| D�� | ��NA��Na+��Na2O�ܽ���1 Lˮ�У�Na+�����ʵ���Ũ��Ϊ1 mol•L-1 |
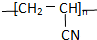 �ĵ�����ȷ���ǣ�������
�ĵ�����ȷ���ǣ�������| A�� | 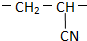 | B�� | CH3-CN | C�� | CH2�TCHCN | D�� | CH2�THCN |
| A�� | 1mol �������ڷ�Ӧ�еõ��ĵ���Ϊ12mol | |
| B�� | Cu��IO3��2����������������ԭ�� | |
| C�� | CuI�и�Ԫ�ػ��ϼ��ڷ�Ӧǰ���� | |
| D�� | I2������������������ԭ���� |
| A�� | �����������������10-4%�Ŀ������������彡�� | |
| B�� | pH��5.6��7.0֮�����ˮͨ����Ϊ���� | |
| C�� | ȼúʱ��������ʯ��ʯ���ɼ��ٷ�����SO2���� | |
| D�� | ���ϳ�ϴ�Ӽ����ڱ�ϸ���ֽ⣬�ʲ��ᵼ��ˮ����Ⱦ |
| A�� | C������ٸı� | |
| B�� | ���ʵ���Ũ��c��A����c��B����c��C����c��D��=m��n��p��q | |
| C�� | �����Ũ�Ȳ��ٸı� | |
| D�� | ��λʱ����m molA�ϼ���ͬʱpmolCҲ�ϼ� |