题目内容
下列制取单质的反应中,化合物作还原剂的是( )
| A、用锌和稀硫酸反应制取氢气 |
| B、用氯气和溴化钠溶液制取溴 |
| C、用碳和高温水蒸气反应制取氢气 |
| D、用氢气和灼热的氧化铜反应制取铜 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:化合物作还原剂,则反应中化合物中某元素的化合价升高,以此来解答.
解答:
解:A.化合物中H元素的化合价降低,作氧化剂,故A不选;
B.化合物中Br元素的化合价升高,作还原剂,故B选;
C.水中H元素的化合价降低,作氧化剂,故C不选;
D.化合物中Cu元素的化合价降低,作氧化剂,故D不选;
故选B.
B.化合物中Br元素的化合价升高,作还原剂,故B选;
C.水中H元素的化合价降低,作氧化剂,故C不选;
D.化合物中Cu元素的化合价降低,作氧化剂,故D不选;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化剂、还原剂判断的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
标准状况下,电解一定物质的量浓度的CuSO4溶液一段时间后,加入0.1mol Cu(OH)2固体使溶液完全恢复到初始状态,则此过程中共产生气体( )
| A、6.72L | B、8.96L |
| C、4.48L | D、5.6L |
已知C(金刚石)=C(石墨)△H=-Q(Q>0),下列热化学方程式放出热量最多的是( )
A、C(金刚石)+
| ||
B、C(石墨)+
| ||
| C、C(金刚石)+O2(g)=CO2(g)△H=-Q3 | ||
| D、C(石墨)+O2(g)=CO2(g)△H=-Q4 |
烷烃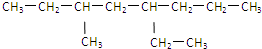 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
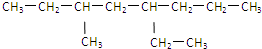 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )| A、1种 | B、2种 | C、3种 | D、4种 |
下列化合物分子中既有离子键又有共价键的是( )
| A、BaCl2 |
| B、Na2O |
| C、(NH4)2SO4 |
| D、H2SO4 |
 ②
② ③CH4 ④?
③CH4 ④? ?⑤
?⑤
 ⑦
⑦ ⑧
⑧
 ⑩
⑩
 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验