题目内容
8.下列混合物的分离或提纯操作不正确的是( )| A. | 除去N2中的少量O2,可通过灼热的Cu网后,收集气体 | |
| B. | 除去FeCl3溶液中Fe(OH)3沉淀可以过滤 | |
| C. | 除去乙醇中的少量NaCl,可用蒸馏的方法 | |
| D. | 重结晶不能用于提纯物质 |
分析 A.Cu与氧气反应,而氮气不反应;
B.过滤分离溶液与沉淀;
C.乙醇易挥发;
D.重结晶可分离溶解度差异较大的可溶性固体.
解答 解:A.Cu与氧气反应,而氮气不反应,则通过灼热的Cu网后,收集气体可除杂,故A正确;
B.过滤分离溶液与沉淀,则除去FeCl3溶液中Fe(OH)3沉淀可以过滤,故B正确;
C.乙醇易挥发,则除去乙醇中的少量NaCl,可用蒸馏的方法,故C正确;
D.重结晶可分离溶解度差异较大的可溶性固体,则重结晶能用于提纯物质,故D错误;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意物质性质的应用,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
16.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 银氨溶液:Na+、K+、NO3-、NH3•H2O | |
| B. | 存在Fe2+的溶液中:Mg2+、SO42-、ClO-、Na+ | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、葡萄糖分子 |
3.Fe、Fe2+、Fe3+三种微粒具有相同的:①质子数 ②中子数 ③核外电子数 ④化学性质( )
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
20.为了探究原电池的电极名称不仅与电极材料有关还与电解质溶液有关,某学生做了如下的实验
根据以上表格内容回答:
(1)实验①中Mg作负极(填“正极”或“负极”),发生氧化反应(填“氧化反应”或“还原反应”).实验③中Mg作正极(填“正极”或“负极”),总反应的离子方程式为:2Al+2OH-+2H2O=AlO2-+3H2↑.
(2)实验②中Al电极上的电极反应式为2H++2e-═H2↑;.
(3)实验④中正极的电极反应式为NO3-+3e-+4H+=NO↑+2H2O.这样构成的原电池与常见的原电池不同,原因是铝在浓硝酸中发生了钝化.
| 编号 | 电极材料 | 电解质溶液 | 电子流向 |
| ① | Mg-Al | HNO3(浓) | Mg→Al |
| ② | Mg-Al | HCl(aq) | Mg→Al |
| ③ | Mg-Al | NaOH(aq) | Al→Mg |
| ④ | Al-Cu | HNO3(浓) | Cu→Al |
(1)实验①中Mg作负极(填“正极”或“负极”),发生氧化反应(填“氧化反应”或“还原反应”).实验③中Mg作正极(填“正极”或“负极”),总反应的离子方程式为:2Al+2OH-+2H2O=AlO2-+3H2↑.
(2)实验②中Al电极上的电极反应式为2H++2e-═H2↑;.
(3)实验④中正极的电极反应式为NO3-+3e-+4H+=NO↑+2H2O.这样构成的原电池与常见的原电池不同,原因是铝在浓硝酸中发生了钝化.
17.下列各组离子在水溶液中一定能大量共存的是( )
| A. | 无色溶液:Al3+、NH4+、Cl-、HCO3- | |
| B. | 使紫色石蕊试纸变红色的溶液:Cl-、NO3-、Fe2+、K+ | |
| C. | 常温下,pH=13的溶液:K+、CO32-、Na+ | |
| D. | c(H+)=0.1mol/L的溶液:CO32-、Na+、HCO3-、Cl- |
18.下列说法中正确的是( )
| A. | 测定溶液的pH值,应先将pH试纸用蒸馏水润湿 | |
| B. | 称量加热后的固体时,均需先将固体在空气中冷却后再称量 | |
| C. | 配制0.1mol/LNa2CO3溶液时,容量瓶应先用0.1mol/L Na2CO3润洗 | |
| D. | 除去铁粉中混有的少量铝粉,可加人过量的氢氧化钠溶液,完全反应后过滤、干燥 |
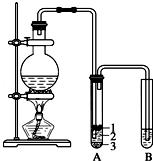 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: ;用E的氧化物和氯化物都能干燥的气体有d
;用E的氧化物和氯化物都能干燥的气体有d