题目内容
下列溶液通入过量的CO2后无沉淀有的( )
| A、CaCl2 |
| B、Ca(ClO)2 |
| C、Na2SiO3 |
| D、饱和Na2CO3溶液 |
考点:氯、溴、碘及其化合物的综合应用,钠的重要化合物
专题:元素及其化合物
分析:A、二氧化碳和氯化钙不反应;
B、碳酸酸性强于次氯酸,二氧化碳能与次氯酸钙反应,但通入过量CO2后无沉淀;
C、硅酸钠可以和碳酸反应生成碳酸钠和硅酸;
D、碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3.
B、碳酸酸性强于次氯酸,二氧化碳能与次氯酸钙反应,但通入过量CO2后无沉淀;
C、硅酸钠可以和碳酸反应生成碳酸钠和硅酸;
D、碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3.
解答:
解:A、盐酸是强酸,碳酸是弱酸,所以碳酸不能制取盐酸,即二氧化碳和氯化钙不反应,最终没有沉淀析出,故A正确;
B、次氯酸是比碳酸还弱的酸,所以二氧化碳、水和次氯酸钙反应生成碳酸钙沉淀,但二氧化碳是过量的,过量的二氧化碳和碳酸钙能继续反应生成可溶性的碳酸氢钙,所以最终没有沉淀析出,故B正确;
C、硅酸钠可以和碳酸反应生成碳酸钠和硅酸,硅酸是白色不溶于水的沉淀,故C错误;
D、碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3而析出,故D错误.
故选:AB.
B、次氯酸是比碳酸还弱的酸,所以二氧化碳、水和次氯酸钙反应生成碳酸钙沉淀,但二氧化碳是过量的,过量的二氧化碳和碳酸钙能继续反应生成可溶性的碳酸氢钙,所以最终没有沉淀析出,故B正确;
C、硅酸钠可以和碳酸反应生成碳酸钠和硅酸,硅酸是白色不溶于水的沉淀,故C错误;
D、碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3而析出,故D错误.
故选:AB.
点评:本题考查了元素及其化合物的性质等,题目难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述错误的是( )
| A、邻二甲苯没有同分异构说明苯不是单双键交替 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、乙烯和苯都能使溴水褪色,褪色的原理相同 |
| D、乙醇、乙酸、苯都能发生取代反应 |
为达到预期的实验目的,下列操作正确的是( )
| A、欲配制质量分数为10%的CuSO4溶液,将l0 g CuSO4?5H2O溶解在90 g水中 |
| B、将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
| C、为区别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| D、用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
一定条件下,在容积固定的某密闭容器中发生的反应N2+3H2?2NH3.在10s内N2的浓度由5mol/L降至4mol/L.下列说法正确的是 ( )
| A、用NH3表示的化学反应速率为0.1 mol/(L?s) |
| B、维持容积的体积不变充入氩气,会加快该反应的速率 |
| C、增加H2的浓度该正反应速率和逆反应速率都会加快 |
| D、反应足够长时间,N2、H2中至少有一种物质浓度降为零 |
下列有机物命名不正确的是( )
A、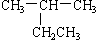 2-甲基丁烷 2-甲基丁烷 |
| B、(CH3)2CHCH2CH2OH 1-戊醇 |
C、CH3- -CH3 1,4-二甲苯 -CH3 1,4-二甲苯 |
D、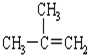 2-甲基丙烯 2-甲基丙烯 |
下列说法正确的是( )
| A、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B、能自发进行的化学反应,一定是△H<0、△S>0 |
| C、焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 |
| D、钢铁发生电化学腐蚀时,负极的电极反应式为 Fe-3e-=Fe3+ |
 图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( )
图中“-”表示相连的物质间在一定条件下可以反应,“-→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图示要求的是( ) 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.