题目内容
17.短周期主族元素W、X、Y、Z的原子序数依次增大,W2-、X+离子具有相同电子层结构,Y的族序数比周期序数大1,W与Z同主族.下列说法正确的是( )| A. | W与X只能形成一种化合物 | B. | X与Z形成的化合物其水溶液呈碱性 | ||
| C. | 氢化物的稳定性:W<Y<Z | D. | Y的最高价氧化物能与水反应 |
分析 短周期主族元素W、X、Y、Z的原子序数依次增大,W2-、X+离子具有相同电子层结构,可知W为O,X为Na;Y的族序数比周期序数大1,Y为第三周期ⅣA族元素,则Y为Si,W与Z同主族,Z为S,以此来解答.
解答 解:由上述分析额裤子,W为O,X为Na,Y为Si,Z为S,
A.W与X能形成氧化钠、过氧化钠等,故A错误;
B.X与Z形成的化合物为硫化钠,其水溶液水解呈碱性,故B正确;
C.非金属性越强,对应氢化物越稳定,则氢化物的稳定性:Y<Z<X,故C错误;
D.Y的最高价氧化物为二氧化硅,与水不反应,故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的位置推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
7.第二周期元素中,其基态原子未成对电子数最多为( )
| A. | 0 | B. | 1 | C. | 2 | D. | 3 |
5.下列选项中的操作、现象与结论完全一致的是( )
| 操作 | 现象 | 结论 | |
| A | 向滴有酚酞的NaOH溶液中通入 Cl2 | 溶液褪色 | HClO有漂白性 |
| B | 无水乙醇与浓硫酸共热至170℃,将产生气体通入溴水 | 溴水褪色 | 乙烯和溴水发生加成反应 |
| C | 向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色深 | 结合H+能力: CO32->HCO3- |
| D | 用发光小灯泡分别做HCl和CH3COOH导电性实验 | 发光强度:HCl强于CH3COOH | CH3COOH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
12.化学与生活、社会发展息息相关,下列说法正确的是( )
| A. | 洗涤剂除油污的原理与热碱液除油污的原理相同 | |
| B. | 食品包装内放置生石灰与放置硅胶的作用相同 | |
| C. | 聚乙烯和聚氯乙烯的单体相同 | |
| D. | 自来水中加入漂白粉与加入硫酸铝的作用相同 |
2.下列关于有机化合物的说法正确的是( )
| A. | 右图为某烃的球棍模型,其分子中C-C键的数目为8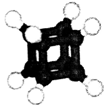 | |
| B. | 由乙烯制取氯乙烷属于取代反应 | |
| C. | C7H7C1属于芳香族化合物的同分异构体有4种 | |
| D. | 丙烯腈(CH2=CH-CN)通过加聚反应制得人造羊毛,其成分与天然羊毛相同 |
9.下列说法正确的是( )
| A. | Fe、A1、Cu均是重要的金属元素,它们的氧化物都是碱性氧化物 | |
| B. | 加热Na2CO3溶液至水分蒸干,可得到NaHCO3和NaOH混合物 | |
| C. | 碳化硅的硬度大、熔点高,是一种高温结构陶瓷 | |
| D. | 工业上用电解熔融MgCl2•6H2O的方法冶炼金属镁 |
6.某溶液仅有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-中的几种.为确定其成分,做如下实验:①取部分溶液.加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀全部溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生.下列推断正确的是( )
| A. | 肯定有Al3+、Cl-,一定没有HCO3-和SO42- | |
| B. | 肯定有Al3+、Mg2+、Cl-,可能有NH4+、K+ | |
| C. | 肯定有Al3+、NH4+、Cl-,肯定没有HCO3- | |
| D. | 该溶液可能显弱酸性,也可能显中性 |
20.下列关于氯气的说法不正确的是( )
| A. | 氯气可用于自来水的消毒 | |
| B. | 氯气制漂白粉时发生的是氧化还原反应 | |
| C. | 氯气可以使湿润的有色布条褪色 | |
| D. | 铁在氯气中燃烧生成氯化亚铁 |