题目内容
9.某同学设计了如下实验测量mg铜银合金样品中铜的质量分数: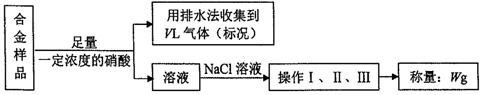
下列说法中不正确的是( )
| A. | 铜、银都能与硝酸反应,收集到的VL气体全为NO | |
| B. | 操作I、II、III分别为过滤、洗涤、干燥 | |
| C. | 利用气体体积VL及样品质量mg可计算铜的质量分数 | |
| D. | 久置的银器变黑、铜绿的形成都发生了氧化还原反应 |
分析 根据流程可知:铜银合金与足量硝酸反应生成硝酸铜、硝酸银溶液、NO或NO2气体,用排水法收集到的VL气体为NO;向反应后的溶液中加入氯化钠溶液,反应生成氯化银沉淀,过滤后得到氯化银固体,然后洗涤、干燥,最后得到干燥的AgCl固体,由此分析解答.
解答 解:A、由流程图可知,实验排水法收集,二氧化氮能与水反应生成NO,故不能金属与硝酸反应生成是NO或NO2或NO、NO2,最后收集的气体为NO,故A正确;
B、根据分析可知,反应生成氯化银沉淀,过滤后得到氯化银固体,然后洗涤、干燥,最后得到干燥的AgCl固体,故B正确;
C、硝酸的浓度不知,合金与硝酸反应放出的气体中可能含有NO2,故C错误;
D、久置的银器发生氧化而变黑、铜在湿润的空气发生氧化生成铜绿,所以都发生氧化还反应,故D正确;
故选C.
点评 本题考查学生对实验原理的理解、物质组成的测定等知识,题目难度中等,理解实验基本操作方法及测定原理为解答关键,需要学生具有扎实的基础知识与综合运用知识分析解决问题的能力.

练习册系列答案
相关题目
9.设NA为阿伏伽德罗常数的数值.下列有关叙述正确的是( )
| A. | pH=1的硫酸溶液中含有的SO42-数目为0.05NA | |
| B. | 100g质量分数为46%的乙醇溶液中所含的氢原子数为12NA | |
| C. | 100mL 1mol/L CH3COONa 溶液中含有的CH3COO-数目为0.1NA | |
| D. | 0.2molNH3与0.3molO2在催化剂的作用下加热充分反应,所得NO的分子数为0.2NA |
20.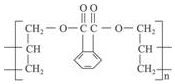 DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
①烯CH2=CH2
②丙烯CH3CH=CH2
③丙烯醇(CH2=CH-CH2OH)
④邻苯二甲酸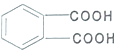
⑤邻苯二甲酸酯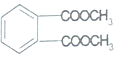
 DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )①烯CH2=CH2
②丙烯CH3CH=CH2
③丙烯醇(CH2=CH-CH2OH)
④邻苯二甲酸

⑤邻苯二甲酸酯

| A. | ①② | B. | ③④ | C. | ②④ | D. | ③⑤ |
17.化学与社会、生活密切相关.下列做法中错误的是( )
| A. | 用食醋浸泡可除去水垢 | |
| B. | 用浓烧碱溶液作蚊虫叮咬处的淸洗剂 | |
| C. | 用明矾溶液的酸性淸除铜镜表面的铜锈 | |
| D. | 用浸泡过高锰酸钾溶液的硅土保存水果 |
4.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(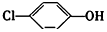 ),同时利用此装置的电能在铁上,下列说法正确的是( )
),同时利用此装置的电能在铁上,下列说法正确的是( )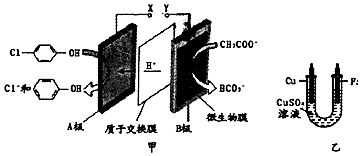
 ),同时利用此装置的电能在铁上,下列说法正确的是( )
),同时利用此装置的电能在铁上,下列说法正确的是( )
| A. | 当外电路中有0.2mol e-转移时,A极区增加的H+的个数为0.2 NA | |
| B. | A极的电极反应式为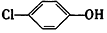 +2e-+H+=Cl-+ +2e-+H+=Cl-+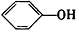 | |
| C. | 乙装置中铁电极应与甲装置中X相连接 | |
| D. | 电镀过程中乙装置中CuSO4溶液浓度逐渐减小 |
14.下列电子式书写正确的是( )
| A. | 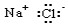 | B. |  | C. | 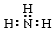 | D. |  |
1.依据元素周期表判断,下列各组关系中正确的是( )
| A. | 稳定性:NH3>H2O>H2S | B. | 氧化性:Cl2>S>P | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 碱性:Mg(OH)2>Ca(OH)2>Ba(OH)2 |
18.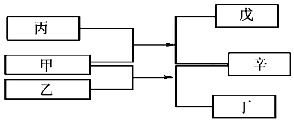 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )| A. | 元素B、C、D的原子半径由大到小的顺序为 r(D)>r(C)>r(B) | |
| B. | 1L0.lmol/L戊溶液中阴离子的总物质的量小于0.1mol | |
| C. | 1mol甲与足量的乙完全反应共转移了约6.02×1023个电子 | |
| D. | 元素的非金属性B>C>A |
19.某老师批阅学生实验报告,下列哪些学生是以科学的态度记录实验数据的( )
| A. | 甲学生用电子天平称取NaOH固体1.220g | |
| B. | 乙学生用广泛pH试纸测定溶液的酸碱性:pH=14.5 | |
| C. | 丙学生用碱式滴定管取25.0mL0.lmol/L的盐酸 | |
| D. | 丁学生用50mL 量筒量取46.70mL浓盐酸 |