题目内容
下列物质分类正确的是( )
| A、福尔马林、水玻璃、氨水均为混合物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳均为电解质 |
| D、SO2、SiO2、CO均为酸性氧化物 |
考点:混合物和纯净物,酸、碱、盐、氧化物的概念及其相互联系,分散系、胶体与溶液的概念及关系,电解质与非电解质
专题:物质的分类专题
分析:混合物是由两种或多种物质混合而成的物质;胶体是分散质粒子直径在1nm-100nm之间的分散系;电解质是在水溶液中或在熔融状态下就能够导电的化合物;酸性氧化物是一类能与水作用生成相应价态的酸或与碱作用生成盐和水或与碱性氧化物反应生成盐的氧化物,且生成物只能有一种盐和水,不可以有任何其它物质生成.
解答:
解:A、福尔马林、水玻璃、氨水均为溶液,既有溶质也有溶剂水,属于混合物,故A正确;
B、氯化铁在水溶液中电离出Fe3+和Cl-,二者的粒子直径均不在在1nm-100nm之间,不属于胶体,故B错误;
C、四氯化碳属于共价化合物不溶于水,在熔融状态下也不能导电,不属于电解质,故C错误;
D、CO不能与水作用生成相应价态的酸,属于不成盐氧化物,故D错误.
故选:A.
B、氯化铁在水溶液中电离出Fe3+和Cl-,二者的粒子直径均不在在1nm-100nm之间,不属于胶体,故B错误;
C、四氯化碳属于共价化合物不溶于水,在熔融状态下也不能导电,不属于电解质,故C错误;
D、CO不能与水作用生成相应价态的酸,属于不成盐氧化物,故D错误.
故选:A.
点评:本题考查混合物、胶体、电解质、酸性氧化物的判别,了解常见物质的组成与构成、抓住各概念的特征进行分析判断是解答此类题的关键.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列物质中由极性键形成的非极性分子是( )
| A、HCl |
| B、Br2 |
| C、CO2 |
| D、Na2O |
能大量共存且溶液为无色透明的离子组是( )
| A、Ag+,K+,NO3-,Cl- |
| B、Na+,H+,NO3-,SO42- |
| C、K+,Ca2+,NO3-,CO32- |
| D、Cu2+,Ba2+,Cl-,SO42- |
下列分子中所有原子都满足最外层8电子结构的是( )
①光气(COCl2) ②SF6 ③HCHO ④BF3 ⑤PCl3 ⑥PCl5 ⑦NO2 ⑧二氟化氙 ⑨N2 ⑩CH4.
①光气(COCl2) ②SF6 ③HCHO ④BF3 ⑤PCl3 ⑥PCl5 ⑦NO2 ⑧二氟化氙 ⑨N2 ⑩CH4.
| A、⑥⑦⑨ | B、①⑤⑨ |
| C、①④⑤⑦ | D、①④⑤⑨ |
比较下列各组粒子半径,正确的是( )
①Cl<Cl-②Mg<Al③Na+<Na④Br<Cl.
①Cl<Cl-②Mg<Al③Na+<Na④Br<Cl.
| A、①和④ | B、只有② |
| C、只有③ | D、①和③ |
若NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2.4g金属镁全部变成镁离子时失去的电子数目为0.1NA |
| B、1.0 mol任何单质气体的分子数均为NA,原子数均为2NA,体积均为22.4L |
| C、17gNH3 所含的原子数目为4NA |
| D、0.5mol/L Na2SO4溶液中含有Na+的数目为NA |
某有机物的分子结构如下所示:CH2=CH-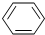 C≡C-CH3,该分子中最多可以有多少个原子共面( )
C≡C-CH3,该分子中最多可以有多少个原子共面( )
 C≡C-CH3,该分子中最多可以有多少个原子共面( )
C≡C-CH3,该分子中最多可以有多少个原子共面( )| A、18 | B、19 | C、20 | D、21 |