题目内容
13.某化学电源的工作原理如图.下列说法不正确的是( )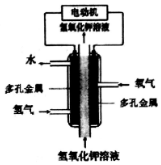
| A. | 采用多孔金属作电极可增大电极接触面积,提高对气体的吸附能力 | |
| B. | 通H2的电极作负极,发生氧化反应 | |
| C. | 通O2的电极发生的电极反应:O2+4e-+4H+=2H2O | |
| D. | 该电池工作时发生的主要能量转化形式为化学能转化为电能和热能 |
分析 碱性氢氧燃料电池中,通入H2的一极为原电池的负极,发生氧化反应,电极反应式为H2-2e-+2OH-=2H2O,通入O2的一极为原电池的正极,发生还原反应,电极反应式为O2+4e-+H2O=4OH-,总反应式为2H2+O2=2H2O,以此解答该题.
解答 解:A.多孔金属作电极,表面积大,具有较强的吸附能力,故A正确;
B.氢气被氧化生成水,发生氧化反应,为原电池负极反应,故B正确;
C.电解质呈碱性,发生O2+4e-+H2O=4OH-,故C错误;
D.原电池工作时,化学能转化为电能,电池发热,有热能的转化,故D正确.
故选C.
点评 本题考查了原电池的工作原理,为高频考点,侧重考查学生的分析能力,注意把握正负极的判断、发生的反应类型、能量的转化、电池反应方程式,题目难度不大.

练习册系列答案
相关题目
3.下列实验设计所得结论不可靠的是( )
| A. | 将电石与水反应产生的气体先通入CuSO4溶液再通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 | |
| B. | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色气体,说明该钾盐是K2CO3或K2SO3 | |
| C. | 将浓硫酸和乙醇溶液共热产生的气体干燥后通入溴的四氯化碳溶液,溶液褪色,说明有乙烯生成 | |
| D. | 将苯、液溴、铁粉混合物反应产生的气体通入到AgNO3溶液中有淡黄色沉淀产生,不能说明有HBr生成 |
4.如果你家里的食用菜油混有水分,你将采用下列何种方法分离( )
| A. | 过滤 | B. | 蒸馏 | C. | 分液 | D. | 萃取 |
1.某芳香族化合物的分子式为C7H6Cl2,该有机物的可能结构有(不考虑立体异构)( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
8.下列说法正确的是( )
| A. | 镁带燃烧可以用CO2灭火 | |
| B. | 单晶硅是重要的半导体材料,常用于制造光导纤维 | |
| C. | Cl2能使湿润的有色布条褪色,是因为Cl2的氧化性 | |
| D. | 金属钠可保存在煤油中 |
18.SO2不具有的性质是( )
| A. | 碱性 | B. | 还原性 | C. | 氧化性 | D. | 漂白性 |
5.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 鸡蛋清溶于水所得澄清液体无丁达尔现象 | |
| B. | 棉、麻、丝、毛完全燃烧都只生成CO2和H2O | |
| C. | 中国瓷器闻名世界,陶瓷的主要成分是SiO2 | |
| D. | 人体内的酶通常通过降低反应的活化能来加快对应反应速率 |
2.吗替麦考酚酯主要用于预防同种异体的器官排斥反应,其结构简式如图所示.下列说法正确的是( )


| A. | 吗替麦考酚酯的分子式为C23H30O7N | |
| B. | 吗替麦考酚酯可发生加成、取代、消去反应 | |
| C. | 吗替麦考酚酯分子中所有碳原子一定处于同一平面 | |
| D. | 1mol吗替麦考酚酯与NaOH溶液充分反应最多消耗3mol NaOH反应 |
17. 实验室测定常温下l molH2的体积通常用如图所示的装置.
实验室测定常温下l molH2的体积通常用如图所示的装置.
实验记录:温度15℃压强1大气压
(1)求得的平均Vm=23.515L/mol;
(2)实验的相对误差为:0.49%%(已知:15℃时Vm的理论值为:Vm=23.631L/mol).
 实验室测定常温下l molH2的体积通常用如图所示的装置.
实验室测定常温下l molH2的体积通常用如图所示的装置.实验记录:温度15℃压强1大气压
| 实验次数 | 镁带质量(g) | 硫酸体积( mL) | 氢气体积( mL) | l摩尔气体的体积(L)(精确到0.001L) |
| 1 | 0.050 | 10 | 49.0 | |
| 2 | 0.049 | 10 | 48.0 |
(2)实验的相对误差为:0.49%%(已知:15℃时Vm的理论值为:Vm=23.631L/mol).