题目内容
德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状.为了验证凯库勒的观点,某学生设计了以下实验方案:

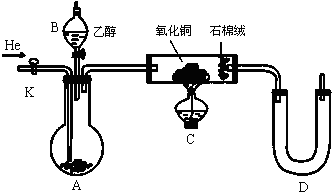
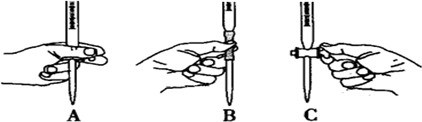
①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;
④待烧瓶C中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象.
(1)A中所发生反应的反应类型为 ,能证明凯库勒观点错误的实验现象是 .
(2)装置B的作用是 .
(3)烧瓶C的容积为500mL,收集气体时,由于空气未排尽,最终水未能充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为37.9,则实验结束后,进入烧杯中的水的体积为 mL(空气的相对分子质量以29计算).

①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;
④待烧瓶C中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象.
(1)A中所发生反应的反应类型为
(2)装置B的作用是
(3)烧瓶C的容积为500mL,收集气体时,由于空气未排尽,最终水未能充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为37.9,则实验结束后,进入烧杯中的水的体积为
考点:性质实验方案的设计
专题:实验设计题
分析:(1)苯与溴在溴化铁做催化剂的条件下发生取代反应,生成溴苯和溴化氢;
(2)由于反应放热,苯和液溴均易挥发,溴的存在干扰检验H+和Br-;
(3)烧瓶中混合气体对H2的相对密度为37.9,故烧瓶中混合气体的平均分子量为37.9×2=75.8,根据平均相对分子质量的计算方法进行计算.
(2)由于反应放热,苯和液溴均易挥发,溴的存在干扰检验H+和Br-;
(3)烧瓶中混合气体对H2的相对密度为37.9,故烧瓶中混合气体的平均分子量为37.9×2=75.8,根据平均相对分子质量的计算方法进行计算.
解答:
解:(1)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,苯分子里的氢原子被溴原子所代替,
方程式为: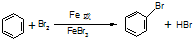 ,该反应为取代反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,
,该反应为取代反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,
故答案为:取代反应;烧瓶C中产生喷泉现象;
(2)由于反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验H+和Br-,
故答案为:吸收挥发出来的苯及溴蒸汽;
(3)烧瓶中混合气体对H2的相对密度为37.9,故烧瓶中混合气体的平均分子量为37.9×2=75.8,
设HBr的体积为x,空气的体积为y,则:
×81+29×
=75.8,x+y=500,解得:x=450mL,y=50mL,
故进入烧瓶中的水的体积为x=450mL,
故答案为:450.
方程式为:
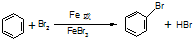 ,该反应为取代反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,
,该反应为取代反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象,故答案为:取代反应;烧瓶C中产生喷泉现象;
(2)由于反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验H+和Br-,
故答案为:吸收挥发出来的苯及溴蒸汽;
(3)烧瓶中混合气体对H2的相对密度为37.9,故烧瓶中混合气体的平均分子量为37.9×2=75.8,
设HBr的体积为x,空气的体积为y,则:
| x |
| 500 |
| y |
| 500 |
故进入烧瓶中的水的体积为x=450mL,
故答案为:450.
点评:本题以实验为载体考查了有机物苯的性质,理清实验原理是解答的关键,题目难度中等.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)??xC(g)+2D(s).2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol/L.下列判断正确的是( )
| A、该条件下此反应的化学平衡常数约为0.91 (L/mol)3 |
| B、A的平均反应速率为0.3mol/(L?s) |
| C、该反应在高温下可以自发进行 |
| D、若混合气体的压强不再改变时,该反应不一定达到平衡状态 |
下列说法正确的是( )
| A、稀H2SO4能导电,所以稀H2SO4是电解质 |
| B、失去电子多的还原剂,还原性一定强 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、根据交叉分类法MgSO4既是镁盐又是硫酸盐 |