题目内容
实验室制取少量N2常利用的反应是NaNO2+NH4Cl
NaCl+N2↑+2H2O,关于该反应的说法正确的是( )
| ||
| A、NaNO2是还原剂 |
| B、生成1molN2时转移的电子为6mol |
| C、NH4Cl中的N元素被氧化 |
| D、N2既是氧化剂又是还原剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:NaNO2+NH4Cl
NaCl+N2↑+2H2O中,N元素的化合价由+3价降低为0,N元素的化合价由-3价升高为0,以此来解答.
| ||
解答:
解:A.NaNO2中N元素的化合价降低,为氧化剂,故A错误;
B.由N元素的化合价变化可知,生成1molN2时转移的电子为3mol,故B错误;
C.NH4Cl中的N元素化合价升高,失去电子被氧化,故C正确;
D.只有N元素的化合价变化,则N2既是氧化产物又是还原产物,而氧化剂、还原剂均为反应物,故D错误;
故选C.
B.由N元素的化合价变化可知,生成1molN2时转移的电子为3mol,故B错误;
C.NH4Cl中的N元素化合价升高,失去电子被氧化,故C正确;
D.只有N元素的化合价变化,则N2既是氧化产物又是还原产物,而氧化剂、还原剂均为反应物,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
下列各项中,正确的是( )
A、Na的原子结构示意图: | ||
| B、N2分子的结构式:N=N | ||
C、HCl的电子式: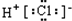 | ||
D、中子数为1的氢原子符号:
|
能源与人类的生活和社会发展密切相关.下列关于能源开发和利用的说法不正确的是( )
| A、人类利用的能源都是通过化学反应获得的 |
| B、煤、石油、天然气是不可再生能源 |
| C、在农村提倡利用沼气作生活燃料 |
| D、未来可用乙醇代替汽油作汽车燃料 |
下列化工方法不属于化学变化的是( )
| A、分馏 | B、裂化 | C、裂解 | D、干馏 |
某烷烃相对分子质量为86,该烷烃的结构简式可能为( )
| A、CH3(CH2)5CH3 |
| B、C(CH3)4 |
| C、(CH3CH2)2CHCH3 |
| D、(CH3)2CHCH2CH3 |
几种短周期元素的原子半径及主要化合价如表,下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、Y最高价氧化物对应的水化物的碱性强于X |
| B、一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C、Y与W形成的化合物具有两性,能溶于浓氨水 |
| D、Y与Z的最高价氧化物对应的水化物能相互反应 |
某有机物的结构简式如图,有关它的说法正确的是( )
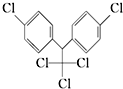

| A、它属于芳香烃 |
| B、该有机物不含官能团 |
| C、分子式为C14H8Cl5 |
| D、1mol该物质能与6mol H2加成 |
下列叙述正确的是( )
| A、ⅠA族元素单质的熔点从上往下逐渐降低 |
| B、分子晶体中一定存在共价键 |
| C、ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| D、同周期非金属氧化物对应的水化物的酸性从左往右依次增强 |