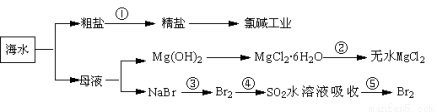
题目内容
一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g),则下列说法正确的是
CH3OCH3(g)+H2O(g),则下列说法正确的是
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 |
|
|
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A、该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
D
【解析】
试题分析:A、比较I与III容器,温度降低,甲醚的物质的量增加,说明降低温度,平衡正向移动,则正向是放热反应,错误;B、该反应是反应前后气体的物质的量不变的可逆反应,恒容条件下,充入一定量的甲醇达到的平衡都是等效平衡,所以容器I与II中甲醇的体积分数相同,错误;C、容器Ⅰ中的温度比容器Ⅱ的温度高,温度越高反应速率越快,达到衡所需时间越短,错误;D、起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,c(CH3OH)=0.1mol/L、c(CH3OCH3 )=0.15mol/L、c(H2O)=0.10mol/L,容器Ⅰ中平衡时c(CH3OCH3)=c(H2O)=0.080mol/1.0L=0.080mol/L,c(CH3OH)=(0.2mol-0.080×2)/1.0L=0.04mol/L,容器Ⅰ中化学平衡常数K1=0.082/0.042=4,浓度商=0.1×0.15/0.1×0.1=1.5<4, 平衡向正反应方向移动,正确,答案选D。
考点:考查了化学平衡常数的有关计算


 (aq),其平衡常数表达式为________。
(aq),其平衡常数表达式为________。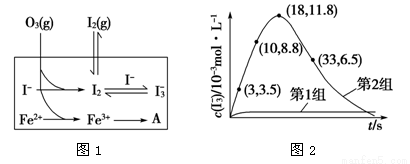

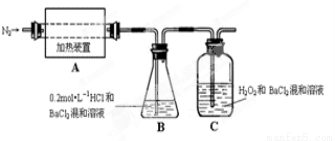
 2Fe2O3?xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3?xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。