题目内容
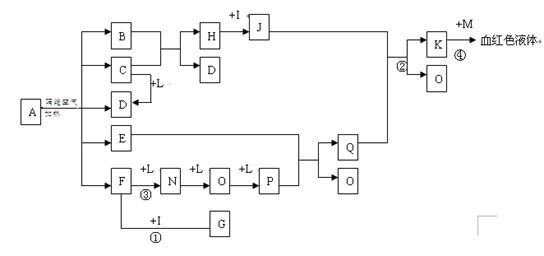
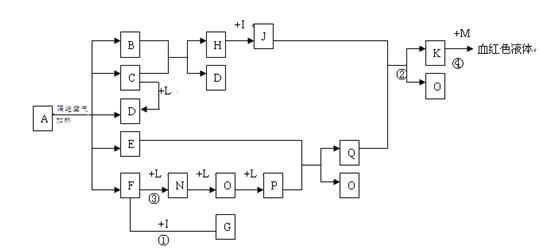
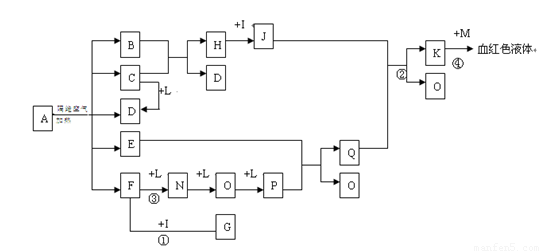
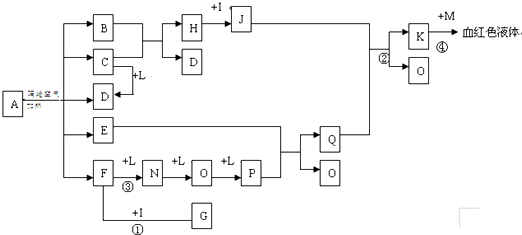
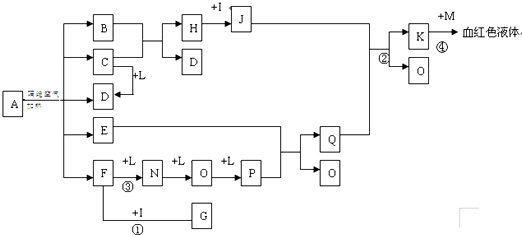
已知A为一无机盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验.
(1)写出G的电子式______,M的化学式______;
(2)写出反应②的离子反应方程式______;
(3)写出反应③的化学反应方程式______;反应①④中属于非氧化还原反应的是______;
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极______
阳极______
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:F=1:2:2:2:2,写出A分解的反应方程式______.
解:依据K与M反应生成血红色溶液,说明K是三价铁盐溶液,M的焰色反应,M为紫色为KSCN;I为常见无氧强酸为盐酸HCl,依据FNOP的转化关系可以推断L为O2,E常温常压下为无色无味的液体推断为H2O,反应①常用于气体F的检验,F和I(HCl)反应,说明F为NH3,G为NH4Cl;F和氧气反应生成的单质N为N2、O为NO,P为NO2,Q为HNO3;依据J和硝酸反应生成的K,是发生氧化还原反应的结果,H和I(HCl)反应推断H为Fe,J为FeCl2,题干中的信息中CD都是无色气体,B+C=Fe+D,能生成铁说明该反应是还原剂还原铁的氧化物生成,所以判断C为CO,D为CO2,B为铁的氧化物.
(1)G为NH4Cl,电子式为: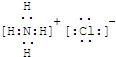 ,M为 KSCN,故答案为:
,M为 KSCN,故答案为: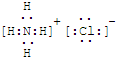 ;KSCN;
;KSCN;
(2)反应②是氯化亚铁被硝酸氧化的反应,离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)反应③是氨气的催化氧化,反应的化学反应方程式:4NH3+3O2=2N2+6H2O; 反应①是氨气和氯化氢生成氯化铵的反应,是非氧化还原反应;④是三价铁离子和硫氰根离子生成络合物的反应,属于非氧化还原反应,故答案为:4NH3+3O2=2N2+6H2O;①④;
(4)石墨电极电解溶液K(Fe3+)时,阴极上是三价铁离子得到电子的过程,电极反应为:Fe3++e=Fe2+;阳极上是溶液中的氯离子失电子发生氧化反应,电极反应为:2Cl--2e=Cl2↑,
故答案为:2Fe3++2e=2Fe2+;2Cl--2e=Cl2↑;
(5)A在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:F=1:2:2:2:2,即B(含铁元素):CO:CO2:H2O:NH3=1:2:2:2:2;依据原子守恒和化合价代数和为0,结合推断中生成物质的性质推断出A的化学式为:(NH4)2Fe(C2O4)2;反应的化学方程式为:(NH4)2Fe(C2O4)2=FeO+2CO↑+2CO2↑+2H2O+2NH3↑,
故答案为:(NH4)2Fe(C2O4)2=FeO+2CO↑+2CO2↑+2H2O+2NH3↑.
分析:依据K与M反应生成血红色溶液,说明K是三价铁盐溶液,M的焰色反应,M为紫色为KSCN;I为常见无氧强酸为盐酸HCl,依据FNOP的转化关系可以推断L为O2,E常温常压下为无色无味的液体推断为H2O,反应①常用于气体F的检验,F和I(HCl)反应,说明F为NH3,G为NH4Cl;F和氧气反应生成的单质N为N2、O为NO,P为NO2,Q为HNO3;依据J和硝酸反应生成的K,是发生氧化还原反应的结果,H和I(HCl)反应推断H为Fe,J为FeCl2,题干中的信息中CD都是无色气体,B+C=Fe+D,能生成铁说明该反应是还原剂还原铁的氧化物生成,所以判断C为CO,D为CO2,B为铁的氧化物;依据判断出的物质进行分析回答问题.
点评:本题考查了物质转化关系和物质性质的综合应用,主要考查金属及其化合物性质的综合应用、氧化还原反应、电解原理的应用、化学方程式的书写、化学式的计算确定,题目难度大.
(1)G为NH4Cl,电子式为:
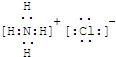 ,M为 KSCN,故答案为:
,M为 KSCN,故答案为: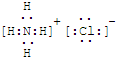 ;KSCN;
;KSCN;(2)反应②是氯化亚铁被硝酸氧化的反应,离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)反应③是氨气的催化氧化,反应的化学反应方程式:4NH3+3O2=2N2+6H2O; 反应①是氨气和氯化氢生成氯化铵的反应,是非氧化还原反应;④是三价铁离子和硫氰根离子生成络合物的反应,属于非氧化还原反应,故答案为:4NH3+3O2=2N2+6H2O;①④;
(4)石墨电极电解溶液K(Fe3+)时,阴极上是三价铁离子得到电子的过程,电极反应为:Fe3++e=Fe2+;阳极上是溶液中的氯离子失电子发生氧化反应,电极反应为:2Cl--2e=Cl2↑,
故答案为:2Fe3++2e=2Fe2+;2Cl--2e=Cl2↑;
(5)A在隔绝空气条件下分解产生的各产物的物质的量之比为B:C:D:E:F=1:2:2:2:2,即B(含铁元素):CO:CO2:H2O:NH3=1:2:2:2:2;依据原子守恒和化合价代数和为0,结合推断中生成物质的性质推断出A的化学式为:(NH4)2Fe(C2O4)2;反应的化学方程式为:(NH4)2Fe(C2O4)2=FeO+2CO↑+2CO2↑+2H2O+2NH3↑,
故答案为:(NH4)2Fe(C2O4)2=FeO+2CO↑+2CO2↑+2H2O+2NH3↑.
分析:依据K与M反应生成血红色溶液,说明K是三价铁盐溶液,M的焰色反应,M为紫色为KSCN;I为常见无氧强酸为盐酸HCl,依据FNOP的转化关系可以推断L为O2,E常温常压下为无色无味的液体推断为H2O,反应①常用于气体F的检验,F和I(HCl)反应,说明F为NH3,G为NH4Cl;F和氧气反应生成的单质N为N2、O为NO,P为NO2,Q为HNO3;依据J和硝酸反应生成的K,是发生氧化还原反应的结果,H和I(HCl)反应推断H为Fe,J为FeCl2,题干中的信息中CD都是无色气体,B+C=Fe+D,能生成铁说明该反应是还原剂还原铁的氧化物生成,所以判断C为CO,D为CO2,B为铁的氧化物;依据判断出的物质进行分析回答问题.
点评:本题考查了物质转化关系和物质性质的综合应用,主要考查金属及其化合物性质的综合应用、氧化还原反应、电解原理的应用、化学方程式的书写、化学式的计算确定,题目难度大.

练习册系列答案
相关题目
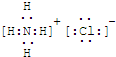
 、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。