题目内容
喹啉(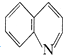 )是一种重要的有机化合物,其合成路线如下:
)是一种重要的有机化合物,其合成路线如下:
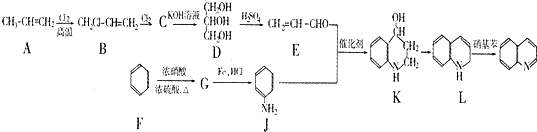
请回答下列问题:
(1)物质D中官能团的名称是 ;由物质K到物质L的反应类型是 .
(2)能用于区别物质A、B的试剂是 .
(3)写出与喹啉同类物质的同分异构体的结构简式 .
(4)写出下列反应的化学方程式:
①F→G: .
②由物质J与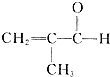 制备物质K的同系物: .
制备物质K的同系物: .
 )是一种重要的有机化合物,其合成路线如下:
)是一种重要的有机化合物,其合成路线如下:
请回答下列问题:
(1)物质D中官能团的名称是
(2)能用于区别物质A、B的试剂是
(3)写出与喹啉同类物质的同分异构体的结构简式
(4)写出下列反应的化学方程式:
①F→G:
②由物质J与
 制备物质K的同系物:
制备物质K的同系物:考点:有机物的合成
专题:有机物的化学性质及推断
分析:A通过CH2═CHCH3
CH2ClCHClCH3转化成B,B与氯气反应生成C、C在氢氧化钾溶液中反应生成丙三醇,则C为CH2ClCHClCH2Cl;F与浓硝酸反应生成G、G转化成J,则G为硝基苯,
(1)根据制备流程可知,D为甘油,含有官能团为羟基;K到L为醇的消去反应;
(2)A为CH2═CHCH3,B为CH2ClCHClCH3,二者区别为B中含有Cl原子,可以通过鉴别卤代烃的方法鉴别二者;
(3)根据同分异构体的书写原则结合有机物 的结构简式书写其结构简式;
的结构简式书写其结构简式;
(4)①G为硝基苯,写出苯与浓硝酸在浓硫酸、加热条件下反应生成硝基苯的反应方程式;
②物质J与 反应生成的K的同系物为:
反应生成的K的同系物为: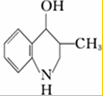 .
.
| Cl2 |
| 高温 |
(1)根据制备流程可知,D为甘油,含有官能团为羟基;K到L为醇的消去反应;
(2)A为CH2═CHCH3,B为CH2ClCHClCH3,二者区别为B中含有Cl原子,可以通过鉴别卤代烃的方法鉴别二者;
(3)根据同分异构体的书写原则结合有机物
 的结构简式书写其结构简式;
的结构简式书写其结构简式;(4)①G为硝基苯,写出苯与浓硝酸在浓硫酸、加热条件下反应生成硝基苯的反应方程式;
②物质J与
 反应生成的K的同系物为:
反应生成的K的同系物为: .
.解答:
解:A通过CH2═CHCH3
CH2ClCHClCH3转化成B,B与氯气反应生成C、C在氢氧化钾溶液中反应生成丙三醇,则C为CH2ClCHClCH2Cl;F与浓硝酸反应生成G、G转化成J,则G为硝基苯,
(1)D为丙三醇,又名甘油,含有官能团为羟基;根据K、L 结构简式可知,K到L为醇的消去反应,故答案为:羟基;消去反应;
(2)A为CH2═CHCH3,B为CH2ClCHClCH3,二者区别为B中含有Cl原子,可以将B与氢氧化钠的水溶液中加热,然后加入稀硝酸中和氢氧化钠至酸性,再加入硝酸银溶液检验溶液中是否生成白色沉淀,有白色沉淀生成的为B,没有生成沉淀的为A,所以选用的试剂为:NaOH水溶液、稀硝酸、硝酸银溶液,
故答案为:NaOH水溶液、稀硝酸、硝酸银溶液;
(3)与 互为同分异构体的同一类物质,可以移动N=C双键的位置,从而得到满足条件的有机物,如
互为同分异构体的同一类物质,可以移动N=C双键的位置,从而得到满足条件的有机物,如 ,故答案为:
,故答案为: ;
;
(4)①F→G的化学方程式为: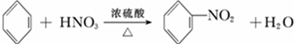 ,故答案为:
,故答案为: ;
;
②由物质J与 生成的物质K的同系物为:
生成的物质K的同系物为: ,该反应的反应方程式为:
,该反应的反应方程式为: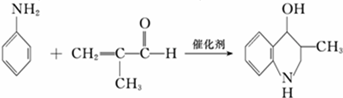 ,故答案为:
,故答案为: .
.
| Cl2 |
| 高温 |
(1)D为丙三醇,又名甘油,含有官能团为羟基;根据K、L 结构简式可知,K到L为醇的消去反应,故答案为:羟基;消去反应;
(2)A为CH2═CHCH3,B为CH2ClCHClCH3,二者区别为B中含有Cl原子,可以将B与氢氧化钠的水溶液中加热,然后加入稀硝酸中和氢氧化钠至酸性,再加入硝酸银溶液检验溶液中是否生成白色沉淀,有白色沉淀生成的为B,没有生成沉淀的为A,所以选用的试剂为:NaOH水溶液、稀硝酸、硝酸银溶液,
故答案为:NaOH水溶液、稀硝酸、硝酸银溶液;
(3)与
 互为同分异构体的同一类物质,可以移动N=C双键的位置,从而得到满足条件的有机物,如
互为同分异构体的同一类物质,可以移动N=C双键的位置,从而得到满足条件的有机物,如 ,故答案为:
,故答案为: ;
;(4)①F→G的化学方程式为:
 ,故答案为:
,故答案为: ;
;②由物质J与
 生成的物质K的同系物为:
生成的物质K的同系物为: ,该反应的反应方程式为:
,该反应的反应方程式为: ,故答案为:
,故答案为: .
.
点评:本题考查有机物的推断与合成,题目难度中等,注意结合烯烃、苯的同系物、氯代烃的性质等知识进行推断,学习中注意相关知识的积累,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
25℃时,在含有大量Ba2+的某澄清透明溶液中,由水电离产生的OH-物质的量浓度为1×10-12mol/L,则在此溶液中还一定能够大量共存的离子组是( )
| A、Na+、Cl-、NO3- |
| B、K+、CH3COO-、SO42- |
| C、NH4+、HCO3-、K+ |
| D、Na+、NO3-、Fe3+ |
用1.0mol?L-1NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积(V)关系如图所示.则原硫酸溶液的物质的量浓度和恰好完全反应后溶液的总体积分别是(设二者混合后体积为二者体积之和)( )

| A、0.5mol?L-1 160mL |
| B、1.0mol?L-1 160mL |
| C、0.5mol?L-1 80mL |
| D、1.0mol?L-180mL |
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞.若再将在成键的C院子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞.则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)

| A、一个金刚石的晶胞中有8个C原子 |
| B、金刚石的密度为3.54g?cm-1 |
| C、在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D、在该种CO2晶胞中含氧原子8个 |
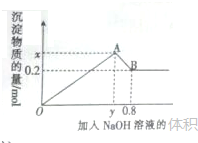 在MgCl2和AlCl3的混合溶液中,逐滴加入1mol?L-1的NaOH溶液直至过量.经测定,加入的NaOH溶液的体积(L)和所得沉淀的物质的量(mol)的关系如图所示.
在MgCl2和AlCl3的混合溶液中,逐滴加入1mol?L-1的NaOH溶液直至过量.经测定,加入的NaOH溶液的体积(L)和所得沉淀的物质的量(mol)的关系如图所示.