题目内容
2.氮及其化合物在工农业生产、生活中有着重要应用,回答下列问题Ⅰ.汽车尾气会影响空气质量,利用催化技术可以将汽车尾气中的NO和CO转变成CO2,其反应为:2NO(g)+2CO(g)?催化剂2CO2(g)+N2(g).
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol•L-1) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol•L-1) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在上述条件下反应能够自发进行,则该反应的△H<0(填写“>”、“<”、“=”).
(2)1至3s的平均反应速率v(N2)=1.42×10-4mol•L-1•s-1,该温度下,反应的平衡常数K=5000L•mol-1
(3)该温度下,在体积恒为10L的三个密闭容器中分别充入下列物质,反应达到平衡后,N2的体积分数最小的是c(填序号)
a.0.1molNO、0.1molCO、0.1molCO2、0.04molN2 b.0.2molNO、0.2molCO c.c0.21molCO2、0.09molN2
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积了提高化学反应速率,为了分别探究温度、催化剂比表面积对对化学反应速率的影响规律(不考虑温度变化对催化剂催化效率的影响),某同学设计了三组探究实验,实验条件及结果见下表:
| 实验编号 | T(℃) | NO初始浓(mol•L-1) | 催化剂的比表面积(m2•g-1) | NO平衡浓度(mol•L-1) |
| 甲 | 280 | 1.80×10-3 | 82 | 0.60×10-3 |
| 乙 | 280 | 1.80×10-3 | 124 | c(乙) |
| 丙 | T(丙) | 1.80×10-3 | 124 | 0.98×10-3 |
Ⅱ.N2H4可作为火箭发射的燃料,NO2作氧化剂,发生反应时生成氮气和气态水,已知2gN2H4(g)完全发生上述反应时共放出35.5kJ热量,试写出该反应的热化学方程式:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1136kJ•mol-1.
如果利用该反应设计成碱性燃料电池,工作时,电池负极的电极反应式为N2H4+4OH--4e-=4H2O+N2↑.
若用该电池做电源使用惰性电极熔融Na2SO4,电解池中阳极的电极反应式为2SO42--4e-=2SO3+O2↑.
分析 Ⅰ.(1)根据反应能够自发进行,则△H-T△S<0来分析该反应的焓变;
(2)根据化学反应速率V=$\frac{△c}{△t}$来计算解答;平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,根据该温度下达化学平衡时各物质平衡时浓度及化学平衡常数的概念来计算;
(3)按化学计量数将已知物质的物质的量转化到方程式右边物质,然后进行比较;
(4)该实验是验证温度、催化剂比表面积对化学反应速率的影响规律,所以甲、乙是只改变催化剂表面积,乙、丙只改变温度;
Ⅱ.根据n=$\frac{m}{M}$计算2gN2H4的物质的量,再根据热化学方程式书写原则书写热化学方程式;肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,用该电池做电源使用惰性电极熔融Na2SO4,电解池中阳极硫酸根离子放电生成三氧化硫和氧气.
解答 解:Ⅰ.(1)因该反应2NO(g)+2CO(g) 2CO2(g)+N2(g)中气体减少,△S<0,由反应能够自发进行,则△H-T△S<0,即该反应一定是放热才有可能自发进行,放热反应中△H<0,
2CO2(g)+N2(g)中气体减少,△S<0,由反应能够自发进行,则△H-T△S<0,即该反应一定是放热才有可能自发进行,放热反应中△H<0,
故答案为:<;
(2)由表格中的数据可知3s内NO浓度的变化量为1.00×10-3-1.50×10-4=8.50×10-4,则υ(NO)=$\frac{8.5×1{0}^{-4}}{3}$mol•L-1•s-1;由化学反应速率之比等于化学计量数之比,则υ(N2)=$\frac{1}{2}$υ(NO)≈1.42×10-4mol•L-1•s-1;
由表格中的数据可知到4s时达到化学平衡,则
2NO+2CO  2CO2 +N2,
2CO2 +N2,
开始(mol/L) 1.00×10-3 3.60×10-3 0 0
转化(mol/L) 9×10-4 9×10-4 9×10-4 4.50×10-4
平衡(mol/L)1.00×10-4 2.70×10-3 9×10-4 4.50×10-4
则平衡常数K=$\frac{C({N}_{2})×{C}^{2}(C{O}_{2})}{{C}^{2}(NO)×{C}^{2}(CO)}$=$\frac{(4.5×1{0}^{-4})×(9×1{0}^{-4})^{2}}{(1.00×1{0}^{-4})^{2}×(2.7×1{0}^{-3})^{2}}$=5000,
故答案为:1.42×10-4;5000;
(3)按化学计量数将已知物质的物质的量转化到方程式右边物质
a.0.1molNO、0.1molCO、0.1molCO2、0.04molN2相当于0.2molCO2、0.09molN2;
b.0.2molNO、0.2molCO 相当于0.2molCO2、0.1molN2;
c.0.21molCO2、0.09molN2;
相同条件下,ab比较,a的N2含量小,ac比较C的N2含量小,
故答案为:C;
(4)该实验是验证温度、催化剂比表面积对化学反应速率的影响规律,则物质的浓度数据相同,只有温度、接触面积两个变量,所以甲、乙是只改变催化剂表面积,c(乙)=0.60×10-3mol•L-1,乙、丙只改变温度,丙组:NO平衡浓度(mol•L-1)=0.98×10-3>0.60×10-3. 该反应正反应为放热,所以丙温度高于甲,
故答案为:>;=;
Ⅱ.2gN2H4的物质的量为$\frac{2g}{32g/mol}$=$\frac{1}{16}$mol,与二氧化氮反应生成氮气与气态水放出35.5kJ的热量,1mol液态肼与足量液态双氧水反应时放出的热量16×35.5kJ=568KJ,则热化学方程式为:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1136kJ•mol-1,
故答案为:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1136kJ•mol-1;
肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2↑,正极发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,若用该电池做电源使用惰性电极熔融Na2SO4,电解池中阳极硫酸根离子放电生成三氧化硫和氧气,电极反应式为:2SO42--4e-=2SO3+O2↑,
故答案为:O2+2H2O+4e-=4OH-;N2H4+4OH--4e-=4H2O+N2↑;2SO42--4e-=2SO3+O2↑.
点评 本题考查较为综合,涉及化学平衡的移动,原电池与电解池等知识,题目难度较大,注意把握电极方程式的书写以及平衡移动原理的应用.

| A. | 不锈钢 | B. | 黄铜 | C. | 生铁 | D. | 水银 |
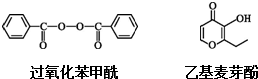
| A. | 过氧化苯甲酰、过氧化钙漂白原理与SO2漂白原理不同 | |
| B. | 1 mol乙基麦芽酚最多能与3 mol H2发生加成反应 | |
| C. | 上述两有机物都能发生取代、加成、氧化和还原反应 | |
| D. | 乙基麦芽酚的一种芳香族同分异构体能发生银镜反应 |
(1)CuSO4溶液和Na2CO3溶液
主要:Cu2++CO32-+H2O═Cu(OH)2↓+CO2↑
次要:Cu2++CO32-═CuCO3↓
(2)CuSO4溶液和Na2S溶液
主要:Cu2++S2-═CuS↓
次要:Cu2++S2-+H2O═Cu(OH)2↓+H2S↑
下列几种物质的溶解度大小的比较中,正确的是( )
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuS>Cu(OH)2>CuCO3 | C. | Cu(OH)2>CuCO3>CuS | D. | Cu(OH)2>CuCO3>CuS |
| A. | 离子交换法淡化海水发生了化学变化 | |
| B. | 海水淡化可为人类提供更多的淡水资源 | |
| C. | 利用太阳能蒸发原理淡化海水属于物理变化 | |
| D. | 将海水中的盐分离出来不能达到海水淡化的目的 |
| A. | 生物柴油是可再生能源 | |
| B. | 发展生物柴油也有益于保护生态环境 | |
| C. | 生物柴油的组成成分与矿物柴油完全相同 | |
| D. | 发展生物柴油有利于调整产业结构、增加农民收入 |
| A. | 25mL量筒 | B. | 25ml酸式滴定管 | C. | 25mL容量瓶 | D. | 胶头滴管 |