题目内容
N2 (g)+3H2 (g)  2NH3(g)? ΔH=-92.4 kJ·mol-1。????????????? 1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示。
2NH3(g)? ΔH=-92.4 kJ·mol-1。????????????? 1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示。
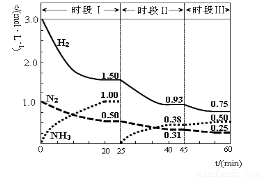
下列说法错误的是:
A.前20分钟反应物的转化率为50%
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
【答案】
C
【解析】
试题分析:H2由浓度3.0mol·L-1变为1.5mol·L-1,N2由1.0mol·L-1变为0.5mol·L-1,都反应了一半,很明显反应物的转化率为50%,A正确;第25分钟可以看到NH3浓度由1.0mol·L-1突然变为0,所以改变的条件是将NH3从反应体系中分离出去,故B正确;时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,相当于增加压强,正向移动,则反应物的转化率增大,平衡常数只跟温度有关,温度没变,平衡常数不变,故C错误;若第60分钟时反应又达到了平衡,氢气、氮气的浓度降低,氨气的浓度增大,说明平衡逆向移动,降低温度符合条件,故D正确;故选C。
考点:考查化学平衡图像。

练习册系列答案
相关题目


 2NH3(g) ;△H< 0 。 400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是(
)
2NH3(g) ;△H< 0 。 400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是(
) 
 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向