题目内容
8.下列物质的保存方法不正确的是( )| A. | 少量金属钠保存在煤油中 | |
| B. | 浓硝酸盛放在无色瓶中 | |
| C. | 少量白磷保存在冷水中 | |
| D. | 氢氧化钠溶液盛放在橡胶塞的试剂瓶中 |
分析 A.钠能与空气中的水和氧气反应,又钠的密度比水略小,比煤油大,与煤油不反应;
B.浓硝酸见光分解;
C.根据白磷易自燃来考虑保存方法;
D.氢氧化钠溶液能够与玻璃塞中的二氧化硅反应.
解答 解:A.少量金属钠保存在煤油中,能够隔绝空气,故A正确;
B.浓硝酸见光分解,应保存在棕色瓶中,故B错误;
C.由于白磷着火点低易自燃,所以要隔绝氧气才行,放到水中即可,故C正确;
D.氢氧化钠溶液能够与玻璃塞中的二氧化硅反应生成具有粘性的硅酸钠,将玻璃塞与玻璃瓶粘在一起,所以可以使用橡皮塞的试剂瓶,故D正确;
故选:B.
点评 本题考查了化学试剂的保存方法判断,注意掌握常见化学试剂的性质及正确的保存方法,明确见光易分解的需要保存在棕色试剂瓶中、与氧气反应的需要隔绝空气密封保存,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列物质中,互为同分异构体的是( )
| A. | 淀粉和纤维素 | B. | 果糖和淀粉 | C. | 蔗糖和果糖 | D. | 果糖和葡萄糖 |
3.下列实验中,利用了盐酸的氧化性的是( )
| A. | 用盐酸除去铜粉中混有的铁粉 | |
| B. | 用浓盐酸和MnO2制氯气 | |
| C. | 用盐酸跟氢氧化钠溶液反应 | |
| D. | 盐酸和硝酸银溶液反应生成白色沉淀 |
13.下列四组物质中,两种分子不具有相同核外电子总数的是( )
| A. | H2O2和HCl | B. | CO和NO | C. | H2O和CH4 | D. | H2S和F2 |
18.氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗.纯化工业级氧化锌(含有Fe(Ⅱ),Mn(Ⅱ),Ni(Ⅱ)等杂质)的流程如下:
工业ZnO $→_{①}^{稀H_{2}SO_{4}}$ 浸出液$→_{适量高锰酸钾溶液②}^{调PH约为5}$$\stackrel{过滤}{→}$滤液$→_{③}^{Zn}$$\stackrel{过滤}{→}$滤液$→_{④}^{Na_{2}CO_{3}}$$\stackrel{过滤}{→}$滤饼$→_{⑤}^{煅烧}$ ZnO
提示:在本实脸条件下,Ni(Ⅱ)不能被氧化:高锰酸钾的还原产物是MnO2,下列说法不正确的是( )
工业ZnO $→_{①}^{稀H_{2}SO_{4}}$ 浸出液$→_{适量高锰酸钾溶液②}^{调PH约为5}$$\stackrel{过滤}{→}$滤液$→_{③}^{Zn}$$\stackrel{过滤}{→}$滤液$→_{④}^{Na_{2}CO_{3}}$$\stackrel{过滤}{→}$滤饼$→_{⑤}^{煅烧}$ ZnO
提示:在本实脸条件下,Ni(Ⅱ)不能被氧化:高锰酸钾的还原产物是MnO2,下列说法不正确的是( )
| A. | 反应②中除掉的杂质离子是Fe2+和Mn2+ | |
| B. | 步骤②加高锰酸钾前若PH较低则Fe2+和Mn2+不能除去 | |
| C. | 反应③的类型为置换反应,滤渣中含有锌和镍 | |
| D. | 反应④中的产物成分可能是ZnCO3.xZn(OH)2若得到干燥滤饼22.4克,煅烧后可得到产品16.2克,则X=2 |
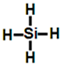 .
.
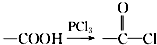 ,请回答以下问题:
,请回答以下问题: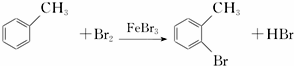 .
.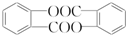 .
.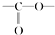 结构
结构