题目内容
乙酰苯胺为无色晶体,具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称.在实验室制备乙酰苯胺常用苯胺与乙酸反应,反应方程式为:
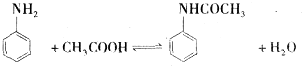
实验的具体操作步骤流程图:

相关的文献数据如下:
据此回答下列问题:
(1)实验时将苯胺、乙酸和锌粉放在单口圆底烧瓶中进行混合加热,所选单口圆底烧瓶的最佳规格是
A.50mL B.100mL C.150mL D.200mL
(2)量筒所接的蒸馏物是 (填化学式).实验这样设计的目的是 .
(3)通过重结晶提纯产物,则乙酰苯胺在水中溶解性的变化特征是 .
(4)对无色片状晶体进行干燥,判断晶体干燥完全的实验方法是 .
(5)锌粉几乎不与纯净的乙酸反应,但随着上述制备乙酰苯胺的反应而会消耗乙酸,原因是 .
(6)实验所得无色片状晶体干燥后称量目标产物质量为4.0g,请计算所得到乙酰苯胺的产率是 .

实验的具体操作步骤流程图:

相关的文献数据如下:
| 试剂名称 | 相对分子质量 | 密度g/mL | 熔点℃ | 沸点℃ | 溶解度 |
| 苯胺 | 93 | 1.02 | -6.2 | 184.4 | 稍溶于水,与乙醇、乙醚、苯混溶 |
| 乙酸 | 60 | 1.05 | 16.7 | 118 | 溶于水、乙醇、乙醚等 |
| 乙酰苯胺 | 135 | 1.21 | 114~116 | 280~290 |
(1)实验时将苯胺、乙酸和锌粉放在单口圆底烧瓶中进行混合加热,所选单口圆底烧瓶的最佳规格是
A.50mL B.100mL C.150mL D.200mL
(2)量筒所接的蒸馏物是
(3)通过重结晶提纯产物,则乙酰苯胺在水中溶解性的变化特征是
(4)对无色片状晶体进行干燥,判断晶体干燥完全的实验方法是
(5)锌粉几乎不与纯净的乙酸反应,但随着上述制备乙酰苯胺的反应而会消耗乙酸,原因是
(6)实验所得无色片状晶体干燥后称量目标产物质量为4.0g,请计算所得到乙酰苯胺的产率是
考点:制备实验方案的设计
专题:实验设计题
分析:(1)圆底烧瓶所盛放的溶液体积一般不能超过烧瓶容积的
,不能低于
;
(2)根据混合物中各物质的沸点分析;根据平衡移动分析;
(3)乙酰苯胺在水中溶解性随着温度的变化而变化;
(4)通过称量固体质量变化来判断判断晶体干燥是否完全;
(5)由于反应中有水生成,纯净乙酸不能电离,有水才会电离出氢离子,反应才可以进行;
(6)5mL苯胺的质量是5mL×1.02g/mol=5.1g,物质的量是
=0.055mol,7.4ml乙酸的质量是7.4ml×1.05g/mol=7.77g,物质的量是
=0.13mol,所以乙酸过量,根据苯胺的物质的量计算出乙酰苯胺的物质的量和质量,再求出产率.
| 2 |
| 3 |
| 1 |
| 3 |
(2)根据混合物中各物质的沸点分析;根据平衡移动分析;
(3)乙酰苯胺在水中溶解性随着温度的变化而变化;
(4)通过称量固体质量变化来判断判断晶体干燥是否完全;
(5)由于反应中有水生成,纯净乙酸不能电离,有水才会电离出氢离子,反应才可以进行;
(6)5mL苯胺的质量是5mL×1.02g/mol=5.1g,物质的量是
| 5.1g |
| 93g/mol |
| 7.77g |
| 60g/mol |
解答:
解:(1)反应物液体的总体积不会超过20mL,由于圆底烧瓶所盛放的溶液体积一般不能超过
,也不能低于
,因此最佳规格是50mL,
故答案为:A;
(2)乙酸、苯胺、乙酰苯胺三者的沸点均高于100℃,水的沸点为100℃,所以水的沸点最低,水最先挥发出来,所以量筒所接的蒸馏物是H2O;有机物没有被蒸发出来,生成物水被蒸发出来,生成物减少平衡正移,则可以提高反应物的转化率,提高产率;
故答案为:H2O;提高产率;
(3)可以通过重结晶提纯产物,乙酰苯胺的溶解度受温度影响较大,在水中溶解性的变化特征是随着温度升高,溶解度迅速增加;
故答案为:随着温度升高,溶解度迅速增加;
(4)对无色片状晶体进行干燥,则可以通过称量固体质量变化来判断判断晶体干燥是否完全,即实验方法是对干燥后的产物进行称量,然后继续干燥一段时间后称量,前后所得质量相等,说明晶体干燥完全;
故答案为:对干燥后的产物进行称量,然后继续干燥一段时间后称量,前后所得质量相等;
(5)锌粉几乎不与纯净的乙酸反应,但随着上述制备乙酰苯胺的反应而会消耗乙酸,这是由于反应中有水生成,纯净乙酸不能电离,有水乙酸会电离出氢离子,反应才可以进行;
故答案为:纯净乙酸不能电离,有水才会电离出氢离子,反应才可以进行;
(6)5ml苯胺的质量是5ml×1.02g/mol=5.1g,物质的量是
=0.055mol,7.4ml乙酸的质量是7.4ml×1.05g/mol=7.77g,物质的量是
=0.13mol,所以乙酸过量,则乙酰苯胺的物质的量等于苯胺的物质的量为0.055mol,则理论上生成产物的质量是0.55mol×135g/mol=7.425g,所以所得到乙酰苯胺的产率是
×100%=54%;
故答案为:54%.
| 2 |
| 3 |
| 1 |
| 3 |
故答案为:A;
(2)乙酸、苯胺、乙酰苯胺三者的沸点均高于100℃,水的沸点为100℃,所以水的沸点最低,水最先挥发出来,所以量筒所接的蒸馏物是H2O;有机物没有被蒸发出来,生成物水被蒸发出来,生成物减少平衡正移,则可以提高反应物的转化率,提高产率;
故答案为:H2O;提高产率;
(3)可以通过重结晶提纯产物,乙酰苯胺的溶解度受温度影响较大,在水中溶解性的变化特征是随着温度升高,溶解度迅速增加;
故答案为:随着温度升高,溶解度迅速增加;
(4)对无色片状晶体进行干燥,则可以通过称量固体质量变化来判断判断晶体干燥是否完全,即实验方法是对干燥后的产物进行称量,然后继续干燥一段时间后称量,前后所得质量相等,说明晶体干燥完全;
故答案为:对干燥后的产物进行称量,然后继续干燥一段时间后称量,前后所得质量相等;
(5)锌粉几乎不与纯净的乙酸反应,但随着上述制备乙酰苯胺的反应而会消耗乙酸,这是由于反应中有水生成,纯净乙酸不能电离,有水乙酸会电离出氢离子,反应才可以进行;
故答案为:纯净乙酸不能电离,有水才会电离出氢离子,反应才可以进行;
(6)5ml苯胺的质量是5ml×1.02g/mol=5.1g,物质的量是
| 5.1g |
| 93g/mol |
| 7.77g |
| 60g/mol |
| 4.0g |
| 7.425g |
故答案为:54%.
点评:本题考查了物质的制备实验方案设计,题目难度中等,侧重于实验能力和数据处理能力的考查,把握实验原理和物质的性质是解题的关键.

练习册系列答案
相关题目
下列反应离子方程式正确的是( )
| A、大理石溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O |
| C、向澄清石灰水中加入少量小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D、氨水中通入过量二氧化硫:2NH3?H2O+SO2=2NH4++SO32-+2H2O |
下列说法中错误的有( )
①、容量瓶用蒸馏水洗净以后,还需要用待配溶液润洗
②、配制950mL 0.5mol?L-1 CuSO4 溶液应选用1000mL 容量瓶
③、定容时仰视刻度线将导致溶液体积偏大,浓度偏低
④、应在天平的左边放上滤纸称量NaOH固体,在右边放砝码
⑤、将烧杯中的溶液小心注入容量瓶后,然后加蒸馏水定容.
①、容量瓶用蒸馏水洗净以后,还需要用待配溶液润洗
②、配制950mL 0.5mol?L-1 CuSO4 溶液应选用1000mL 容量瓶
③、定容时仰视刻度线将导致溶液体积偏大,浓度偏低
④、应在天平的左边放上滤纸称量NaOH固体,在右边放砝码
⑤、将烧杯中的溶液小心注入容量瓶后,然后加蒸馏水定容.
| A、①②③ | B、①②⑤ |
| C、①④⑤ | D、③④⑤ |
“秦砖汉瓦”是我国传统建筑文化的一个缩影.同是由黏土烧制的砖瓦,有的是黑色的,有的却是红色的,你猜测其中的原因可能( )
| A、土壤中含有铁粉、二氧化锰等 |
| B、黑砖瓦是煅烧过程中附着了炭黑,红砖则是添加了红色耐高温染料 |
| C、土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu或Cu2O |
| D、土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色Fe304或FeO和红色Fe2O3 |
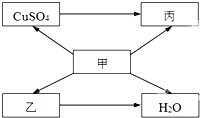 甲、乙、丙为初中化学常见物质,其中乙为胃液中的一种酸.他们相互转化关系如图所示(“→”表示物质变化,部分反应条件和部分生成物已省略).
甲、乙、丙为初中化学常见物质,其中乙为胃液中的一种酸.他们相互转化关系如图所示(“→”表示物质变化,部分反应条件和部分生成物已省略).