题目内容
下列实验中,能发生化学反应且反应完成后没有沉淀生成的是
- A.向装有银粉的试管中滴加足量稀氨水
- B.向Na2SiO3溶液中加入足量盐酸
- C.向CaCl2和CH3COOH的混合溶液中加入少量Na2CO3粉末
- D.向溶有SO2的BaCl2溶液中加入足量NaOH溶液
C
分析:复分解反应的条件:有气体生成、有沉淀生成、或是有难电离的物质生成,只要具备条件之一反应才可以发生,可以根据物质的性质来回答.
解答:A、金属银和氨水不发生反应,不合题意,故A错误;
B、Na2SiO3溶液中加入足量盐酸生成白色沉淀硅酸和氯化钠溶液,即能发生化学反应且反应完成后有沉淀生成,不合题意,故B错误;
C、向CaCl2和CH3COOH的混合溶液中加入少量Na2CO3粉末,碳酸钠和氯化钙会生成碳酸钙沉淀,但是碳酸钙会和醋酸发生反应生成醋酸钙溶液和水,即能发生化学反应且反应完成后没有沉淀生成,符合题意,故C正确;
D、向溶有SO2的BaCl2溶液中加入足量NaOH溶液后,二氧化硫会和氢氧化钠反应生成亚硫酸钠,在氢氧化钠足量的情况下,能和BaCl2溶液发生反应生成亚硫酸钡沉淀,不合题意,故D错误.
故选C.
点评:本题考查学生物质的性质以及复分解反应发生的条件,可以根据所学知识来回答,难度不大.
分析:复分解反应的条件:有气体生成、有沉淀生成、或是有难电离的物质生成,只要具备条件之一反应才可以发生,可以根据物质的性质来回答.
解答:A、金属银和氨水不发生反应,不合题意,故A错误;
B、Na2SiO3溶液中加入足量盐酸生成白色沉淀硅酸和氯化钠溶液,即能发生化学反应且反应完成后有沉淀生成,不合题意,故B错误;
C、向CaCl2和CH3COOH的混合溶液中加入少量Na2CO3粉末,碳酸钠和氯化钙会生成碳酸钙沉淀,但是碳酸钙会和醋酸发生反应生成醋酸钙溶液和水,即能发生化学反应且反应完成后没有沉淀生成,符合题意,故C正确;
D、向溶有SO2的BaCl2溶液中加入足量NaOH溶液后,二氧化硫会和氢氧化钠反应生成亚硫酸钠,在氢氧化钠足量的情况下,能和BaCl2溶液发生反应生成亚硫酸钡沉淀,不合题意,故D错误.
故选C.
点评:本题考查学生物质的性质以及复分解反应发生的条件,可以根据所学知识来回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
| |||||||||||||||||||||||||||||





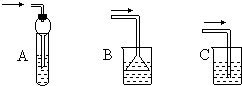 实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为:
实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得.反应的化学方程式为: