题目内容
下列电子式书写正确的是( )
A、氯化钠 |
B、氨气 |
C、氯化钙 |
D、硫化钠 |
考点:电子式
专题:化学用语专题
分析:A.氯化钠为离子化合物,钠离子和氯离子都需要标出所带电荷;
B.氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对;
C.氯化钙为离子化合物,相同的阴离子应分开写;
D.硫化钠为离子化合物,阴离子硫离子需要标出最外层电子,阳离子钠离子分开写.
B.氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对;
C.氯化钙为离子化合物,相同的阴离子应分开写;
D.硫化钠为离子化合物,阴离子硫离子需要标出最外层电子,阳离子钠离子分开写.
解答:
解:A.氯化钠为离子化合物,其电子式中需要标出阴阳离子所带电荷,氯化钠的电子式为Na+[:
:]-,故A错误;
B.氨气为共价化合物,氮原子最外层达到8个电子稳定结构,正确达到电子式为: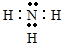 ,故B错误;
,故B错误;
C.氯化钙为离子化合物,相同的阴离子应分开写,电子式为: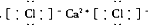 ,故C错误;
,故C错误;
D.硫化钠为离子化合物,阴离子硫离子需要标出最外层电子,阳离子钠离子分开写,电子式为: ,故D正确;
,故D正确;
故选D.
| ||
| .. |
B.氨气为共价化合物,氮原子最外层达到8个电子稳定结构,正确达到电子式为:
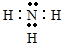 ,故B错误;
,故B错误;C.氯化钙为离子化合物,相同的阴离子应分开写,电子式为:
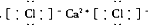 ,故C错误;
,故C错误;D.硫化钠为离子化合物,阴离子硫离子需要标出最外层电子,阳离子钠离子分开写,电子式为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了电子式的书写判断,题目难度中等,注意掌握电子式的概念及正确表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别

练习册系列答案
相关题目
下列表达方式不正确的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式  | ||
C、S2-离子的结构示意图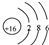 | ||
D、镁-24原子
|
下列化工生产过程所发生的反应不属于氧化还原反应的是( )
| A、用氯气和消石灰制漂白粉 |
| B、用纯碱、石灰石和石英制普通玻璃 |
| C、用石油炼制过程脱硫得到的硫磺制造硫酸 |
| D、用金属钠从四氯化钛(TiCl4)中提炼金属钛 |
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子的外围电子排布式为3s23p6的是( )
| A、W2- |
| B、X+ |
| C、Y3- |
| D、Z2- |
设阿伏加德罗常数的值为NA,下列叙述正确的是( )
A、常温下,1L 0.1mol?L-1的NH4NO3溶液中NH
| ||
| B、常温下,4.4g CO2和N2O混合物中所含有的原子数为0.3NA | ||
| C、标准状况下,2.24L乙烷中含有的非极性键数为0.7NA | ||
| D、1molCl2与足量的氢氧化钠溶液反应转移的电子数为2NA |
C4H10在光照条件下与氯气发生取代反应可生成C4H9Cl,C4H8Cl2等一系列氯代烃,下列有关叙述中正确的是( )
| A、C4H10的同分异构体共有3种 |
| B、C4H9Cl的同分异构体共有3种 |
| C、C4H8Cl2的同分异构体共有6种 |
| D、生成的氯代烃中可能含有CH(CCl3)3 |
下列说法正确的是( )
| A、化学反应不一定都有反应热 |
| B、使用催化剂可以改变反应的平衡常数 |
| C、升高温度使反应加快,是因为降低了反应的活化能 |
| D、对于同一个化学反应无论是一步完成还是分几步完成,其反应的焓变相同 |
常温下,下列溶液pH小于7的是( )
| A、CH3COONa |
| B、CuSO4 |
| C、NaHCO3 |
| D、Na2CO3 |
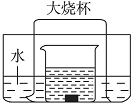 如图所示的实验装置,向盛有足量水的水槽里放两个烧杯,小烧杯里放有适量的铜片和过量的浓硝酸,小烧杯外面倒扣一个大烧杯,请回答下列问题:
如图所示的实验装置,向盛有足量水的水槽里放两个烧杯,小烧杯里放有适量的铜片和过量的浓硝酸,小烧杯外面倒扣一个大烧杯,请回答下列问题: