题目内容
已知8gA能与32gB恰好完全反应,生成22gC和一定量D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量C,则D的摩尔质量为 .
考点:质量守恒定律,摩尔质量
专题:计算题
分析:8gA能与32gB恰好完全反应,生成22gC和一定量D,根据质量守恒,生成D的质量为8g+32g-22g=18g,故A、B、C、D按质量比8g:32g:22g:18g=4:16:11:9进行反应,据此进行16gA与70gB反应的过量计算,再根据质量比计算生成的D的质量,利用M=
计算D的摩尔质量.
| m |
| n |
解答:
解:8gA能与32gB恰好完全反应,生成22gC和一定量D,根据质量守恒D的质量为8g+32g-22g=18g,故A、B、C、D按质量比8g:32g:22g:18g=4:16:11:9进行反应,16gA完全反应需要B的质量为16g×
=64g<70g,故B过量,则生成的D的质量为16g×
=36g,故D的摩尔质量为
=18g/mol;
故答案为:18g/mol.
| 16 |
| 4 |
| 9 |
| 4 |
| 36g |
| 2mol |
故答案为:18g/mol.
点评:本题考查质量守恒定律、摩尔质量计算,比较基础,关键是确定反应中各物质的质量定比关系.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
某芳香烃的分子式为C9H10,它能使溴水褪色,符合上述条件的芳香烃有( )
| A、5种 | B、6种 | C、3种 | D、2种 |
对下列实验过程的评价,正确的是( )
| A、某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐 |
| B、某溶液中先滴加稀盐酸酸化,再滴加几滴BaCl2溶液,生成白色沉淀,证明一定含有SO42- |
| C、某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性 |
| D、验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含有Cl- |
有8种物质:①乙烷;②乙烯;③聚1,3-丁二烯;④苯;⑤2-丁炔;⑥溴乙烷;⑦聚丙烯;⑧环己烯;⑨邻二甲苯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A、①③⑤⑦ | B、①③④⑧ |
| C、①④⑥⑦ | D、②③⑤⑧ |
聚合物 的单体是( )
的单体是( )
 的单体是( )
的单体是( )A、 |
| B、CH2=CH2 |
C、 |
D、 |
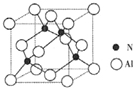 氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
氮的化合物在无机化工领域有着重要的地位.请回答下列问题: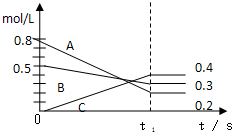 一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.依图中数据回答.
一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.依图中数据回答.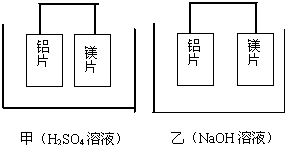 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图: