题目内容
14.如图是利用二甲苯的一种同分异构体制备新型染料M的合成路线图.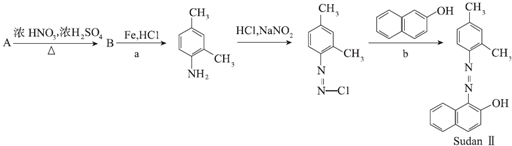
(1)a反应所属反应类型为还原反应,b反应生成另一小分子是HCl.
(2)写出B的结构简式
 .
.(3)C与A互为同分异构体,含有两个不相邻的取代基,C的一氯取代产物最多可能有2种;D是其中一种,苯环上含有三个取代基,D与酸性高锰酸钾反应得E,E在一定条件下能与乙二醇反应生成高分子化合物F,F是一种优良的高分子材料.写出下列反应的化学方程式:①E与过量热NaOH溶液反应
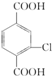 +4NaOH→
+4NaOH→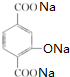 +NaCl+3H2O.②E→F
+NaCl+3H2O.②E→F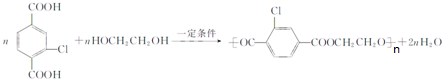 .
.(4)新型染料M在一定条件下可降解生成
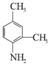 和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为8.8%.
和另一种含氮有机分子G,G分子既能与氢氧化钠溶液反应,也能与盐酸反应.G分子中氮元素的质量分数为8.8%.
分析 A为二甲苯的一种同分异构体,发生硝化反应生成B,B中硝基还原为氨基,结合B的还原产物结构简式可知A为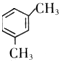 ,B为
,B为 .比较
.比较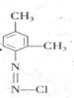 和
和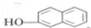 以及SudanⅡ的结构,可知b为取代反应,反应b生成的小分子为HCl;
以及SudanⅡ的结构,可知b为取代反应,反应b生成的小分子为HCl;
C与A互为同分异构体,且有两个不相邻的取代基,说明C为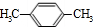 ,为高对称结构,苯环上只有一种氢,甲基上一种氢,故其一氯取代物有2种;D是对二甲苯苯环上取代的一氯取代物,酸性高锰酸钾可将苯环上的甲基氧化为羧基,即E为
,为高对称结构,苯环上只有一种氢,甲基上一种氢,故其一氯取代物有2种;D是对二甲苯苯环上取代的一氯取代物,酸性高锰酸钾可将苯环上的甲基氧化为羧基,即E为 .E与乙二醇发生缩聚反应生成F为
.E与乙二醇发生缩聚反应生成F为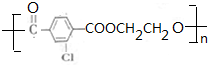 ;
;
比较M和 的结构简式,可知G的结构简式为
的结构简式,可知G的结构简式为 ,其分子式是C10H9NO.
,其分子式是C10H9NO.
解答 解:(1)A为二甲苯的一种同分异构体,发生硝化反应生成B,a过程B中硝基转化为氨基,a反应过程是去氧加氢的反应,属于还原反应,
比较 和
和 以及SudanⅡ的结构,可知b为取代反应,反应b生成的小分子为HCl,
以及SudanⅡ的结构,可知b为取代反应,反应b生成的小分子为HCl,
故答案为:还原反应;HCl;
(2)结合B的还原产物结构简式可知A为 ,A发生硝化反应生成B为
,A发生硝化反应生成B为 ,
,
故答案为: ;
;
(3)C与A互为同分异构体,且有两个不相邻的取代基,说明C为 ,为高对称结构,苯环上只有一种氢,甲基上一种氢,故其一氯取代物有2种;D是对二甲苯苯环上取代的一氯取代物,酸性高锰酸钾可将苯环上的甲基氧化为羧基,即E为
,为高对称结构,苯环上只有一种氢,甲基上一种氢,故其一氯取代物有2种;D是对二甲苯苯环上取代的一氯取代物,酸性高锰酸钾可将苯环上的甲基氧化为羧基,即E为 .
.
①E与氢氧化钠反应时,苯环上的卤原子将发生水解反应,生成酚羟基,并能与氢氧化钠反应,生成酚钠,羧基也与氢氧化钠反应,反应方程式为: +4NaOH→
+4NaOH→ +NaCl+3H2O,
+NaCl+3H2O,
②E与乙二醇发生缩聚反应生成F为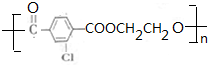 ,反应方程式为:
,反应方程式为: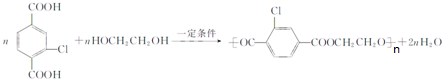 ,
,
故答案为:2; +4NaOH→
+4NaOH→ +NaCl+3H2O;
+NaCl+3H2O;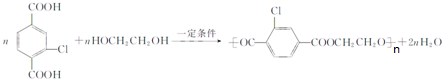 ;
;
(4)比较M和 的结构简式,可知G的结构简式为
的结构简式,可知G的结构简式为 ,其分子式是C10H9NO,氮元素的质量分数为$\frac{14}{159}$×100%=8.8%,
,其分子式是C10H9NO,氮元素的质量分数为$\frac{14}{159}$×100%=8.8%,
故答案为:8.8%.
点评 本题考查有机物的推断与机合成、反应类型、同分异构体、有机反应方程式书写等,书写缩聚反应方程式注意原子守恒,熟练掌握官能团的性质与转化.

| A. | 工业采用火法炼铜:Cu2S+O2=2Cu+SO2 每生成2mol铜,反应共转移4NA个电子 | |
| B. | 7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.1NA | |
| C. | CO2通过Na2O2使其增重bg时,反应中转移的电子数为$\frac{b{N}_{A}}{44}$ | |
| D. | 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.02NA |
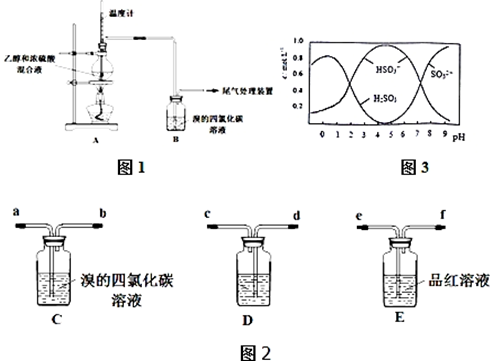
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
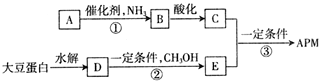
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp=1×10-10,Ksp=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全,此时溶液中c(SO32-)≤0.05mol•L-1.
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| B | 乙酸乙酯(乙酸) | KOH溶液.水 | 分液 |
| C | CO2(CO) | CuO粉末 | 通过灼热的CuO粉末 |
| D | SiO2(Al2O3) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 25℃时,1L pH=11的CH3COONa溶液中水电离出的OH-的数目为0.001NA | |
| B. | 28g乙烯和丙烯的混合气体含有的原子个数为3NA | |
| C. | 1mol•L-1 NaHCO3溶液中含有HCO3数目小于NA | |
| D. | 1mol Cl2与足量NaOH溶液反应时转移电子数为2NA |
| A. | 64gSO2含有硫原子数为2NA | |
| B. | NA个氧分子和NA个氢分子的质量比等于16:1 | |
| C. | 28g氮气所含的原子数目为NA | |
| D. | 标准状况下,22.4L的水含有 NA个水分子 |
| A. | 汞可与稀硫酸反应生成氢气 | |
| B. | 丹砂在空气中灼烧发生了分解反应 | |
| C. | 水银在空气中继续加热又生成硫化汞 | |
| D. | 水银温度计打碎时,立即用纸槽收集洒落的汞珠即可 |
| A. | Mg2+、Al3+、Cl-、OH- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | K+、NH4+、CO32-、OH- |
 .C中所含官能团的名称为羧基、氨基.
.C中所含官能团的名称为羧基、氨基. .
.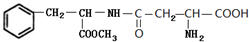 和
和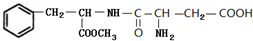 .
.