题目内容
25℃时,下列各溶液中有关物质的量浓度关系正确的是( )
| A、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)>c(OH-)+c(CH3COO-) |
| B、Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、NH4HSO4溶液中滴加NaOH溶液至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| D、pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(C6H5ONa )>c(NaOH ) |
考点:离子浓度大小的比较
专题:
分析:A.混合液中一定满足电荷守恒,根据电荷守恒判断;
B.碳酸钠溶液中满足物料守恒,根据碳酸钠溶液中的物料守恒判断;
C.硫酸氢铵与氢氧化钠按照物质的量1:1反应时生成硫酸铵、硫酸钠溶液,混合液显示酸性,则需要加入的氢氧化钠的物质的量大于硫酸氢铵;
D.pH相同,碱溶液的浓度最小,水解程度越小的盐溶液浓度越大,根据盐的水解及其影响进行判断.
B.碳酸钠溶液中满足物料守恒,根据碳酸钠溶液中的物料守恒判断;
C.硫酸氢铵与氢氧化钠按照物质的量1:1反应时生成硫酸铵、硫酸钠溶液,混合液显示酸性,则需要加入的氢氧化钠的物质的量大于硫酸氢铵;
D.pH相同,碱溶液的浓度最小,水解程度越小的盐溶液浓度越大,根据盐的水解及其影响进行判断.
解答:
解:A.醋酸与氢氧化钠溶液反应,无论溶液显示酸性、中性还是碱性,一定满足电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),故A错误;
B.Na2CO3溶液中一定满足物料守恒,根据物料守恒可得:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.NH4HSO4溶液中滴加NaOH溶液至溶液恰好呈中性,当硫酸氢铵与氢氧化钠物质的量相等时,反应生成硫酸铵和硫酸钠,溶液显示酸性,则加入的氢氧化钠应该稍稍过量,则:c(Na+)>c(SO42-),溶液中离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故C正确;
D.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,氢氧化钠为强碱溶液,则其浓度最小;水解程度大小为:Na2CO3>C6H5ONa>CH3COONa,则pH相同时溶液浓度大小为:Na2CO3<C6H5ONa<CH3COONa,所以相同pH时溶液浓度大小为:c(CH3COONa)>c(C6H5ONa )>c(Na2CO3)>c(NaOH ),故D错误;
故选C.
B.Na2CO3溶液中一定满足物料守恒,根据物料守恒可得:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.NH4HSO4溶液中滴加NaOH溶液至溶液恰好呈中性,当硫酸氢铵与氢氧化钠物质的量相等时,反应生成硫酸铵和硫酸钠,溶液显示酸性,则加入的氢氧化钠应该稍稍过量,则:c(Na+)>c(SO42-),溶液中离子浓度大小为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故C正确;
D.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,氢氧化钠为强碱溶液,则其浓度最小;水解程度大小为:Na2CO3>C6H5ONa>CH3COONa,则pH相同时溶液浓度大小为:Na2CO3<C6H5ONa<CH3COONa,所以相同pH时溶液浓度大小为:c(CH3COONa)>c(C6H5ONa )>c(Na2CO3)>c(NaOH ),故D错误;
故选C.
点评:本题考查了溶液中离子浓度大小比较,题目难度中等,注意掌握溶液中电荷守恒、物料守恒、质子守恒等知识的含义,明确比较溶液中离子浓度大小的方法,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )
可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、m+n>p |
| C、增大压强平衡向正反应方向移动 |
| D、升高温度平衡向正反应方向移动 |
下列说法中正确的是( )
| A、平衡常数的大小与起始浓度有关 |
| B、K值越大,反应物的转化率越小 |
| C、K值越大,反应物的转化率越大 |
| D、温度越高,K值越大 |
在O.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH≒CH3COO-+H+对于该平衡,下列叙述正确的是
( )
( )
| A、加入少量CH3COONa固体,平衡向正反应方向移动 |
| B、加水,反应速率变小,平衡向正反应方向移动 |
| C、滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 |
| D、加入少量NaOH固体,平衡向逆反应方向移动 |
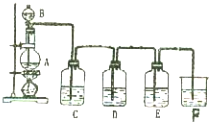 实验室用图所示装置制备氯气,并进行氯气性质实验,请回答下列问题:
实验室用图所示装置制备氯气,并进行氯气性质实验,请回答下列问题: