题目内容
已知常温下:KSP (AgCl)=1.8×10-10 mol2?L-2,KSP (Ag2CrO4)=1.9×10-12 mol3?L-3,下列叙述正确的是( )
| A、AgCl在饱和NaCl溶液中的 KSP比在纯水中的 KSP 小 |
| B、向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP (AgCl)<KSP (AgI) |
| C、将0.001 mol?L-1 的AgNO3溶液滴入0.001 mol?L-1 的KCl和0.001 mol?L-1 的K2CrO4 溶液中先产生Ag2CrO4沉淀 |
| D、向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.KSP只于温度有关;
B.从难溶电解质的溶解平衡的角度分析;
C.根据KSP计算,如生成沉淀,应满足Qc>KSP;
D.银离子与氨水生成氢氧化二氨合银.
B.从难溶电解质的溶解平衡的角度分析;
C.根据KSP计算,如生成沉淀,应满足Qc>KSP;
D.银离子与氨水生成氢氧化二氨合银.
解答:
解:A.KSP只于温度有关,与溶液中离子浓度无关.故A错误;
B.沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)>KSP(AgBr).故B错误;
C.将0.001 mol?L-1的AgNO3溶液滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4溶液中,
已知c(Ag+)×c(Cl-)=1.8×10-10,则c(Ag+)=1.8×10-7 mol/L,
而c2(Ag+)×c(CrO42-)=1.9×10-12,则c(Ag+)=4.35×10-5mol/L,AgCl先达到饱和,应先生成AgCl沉淀,故C错误;
D.银离子与氨水生成氢氧化二氨合银,使平衡向右移动.故D正确.
故选D.
B.沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)>KSP(AgBr).故B错误;
C.将0.001 mol?L-1的AgNO3溶液滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4溶液中,
已知c(Ag+)×c(Cl-)=1.8×10-10,则c(Ag+)=1.8×10-7 mol/L,
而c2(Ag+)×c(CrO42-)=1.9×10-12,则c(Ag+)=4.35×10-5mol/L,AgCl先达到饱和,应先生成AgCl沉淀,故C错误;
D.银离子与氨水生成氢氧化二氨合银,使平衡向右移动.故D正确.
故选D.
点评:本题综合考查难溶电解质的溶解平衡,为高频考点,侧重于计算以及概念理解的考查,题目难度中等,注意把握计算公式的应用.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案
相关题目
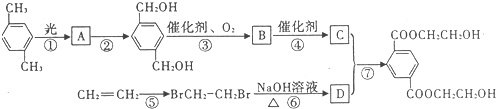
在下列条件下能制得括号中物质的是( )
A、苯在常温下与浓硝酸混合(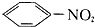 ) ) |
| B、将乙烯通入到水中(CH3CH2OH) |
C、甲苯与氯气在氯化铁催化下反应( ) ) |
| D、乙醇在银催化下加热与氧气反应(CH3CHO) |
用下列实验装置进行相应实验,能达到实验目的是-玻璃棒( )
A、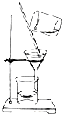 用如图所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质 |
B、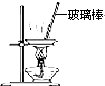 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
C、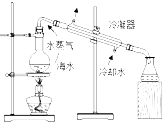 用如图所示装置从海水制取蒸馏水 |
D、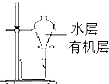 用如图所示装置分离酒精萃取碘水中的碘 |




 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.请回答: