题目内容
2.下列说法不正确的是(NA为阿伏加德罗常数)( )| A. | 46 g N2O4和NO2的混合物含原子总个数为3 NA | |
| B. | 钠在空气中燃烧可生成多种氧化物,则23g钠充分燃烧时转移电子数为1NA | |
| C. | 1 L 0.1 mol/L的KHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| D. | 60 g Si02中含Si-O键的个数为4 NA |
分析 A、N2O4和NO2的最简式均为NO2;
B、求出钠的物质的量,然后根据反应后钠元素为+1价来分析;
C、HCO3-在溶液中既能水解为H2CO3又能电离为CO32-,根据物料守恒来分析;
D、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析.
解答 解:A、N2O4和NO2的最简式均为NO2,故46g混合物中含有的NO2的物质的量为n=$\frac{46g}{46g/mol}$=1mol,故含有3mol原子即3NA个,故A正确;
B、23g钠的物质的量为1mol,而反应后钠元素为+1价,故1mol钠转移1mol电子即NA个,故B正确;
C、HCO3-在溶液中既能水解为H2CO3又能电离为CO32-,根据物料守恒可知,溶液中H2CO3、HCO3-和CO32-离子数之和为0.1NA个,故C错误;
D、60g二氧化硅的物质的量为n=$\frac{60g}{60g/mol}$=1mol,而1mol二氧化硅中含4mol硅氧键,即4NA个,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
12.已知2SO2(g)+O2(g)?2SO3(g)△H=-167kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO2、1molO2和1molSO3、1molSO2、0.5mol当它们分别达到平衡时放出的热量为Q1和Q2KJ,则下列比较正确的是( )
| A. | Q2=$\frac{1}{2}$ Q1=98.5 | B. | Q2=$\frac{1}{2}$ Q1<98.5 | C. | Q2<$\frac{1}{2}$ Q1<98.5 | D. | $\frac{1}{2}$Q1<Q2<98.5 |
13.以结构式表示的下列各物质中,属于烷烃的是( )
| A. |  | B. |  | C. |  | D. |  |
10.生活中常用到一些化学知识,下列说法中不正确的( )
| A. | 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于水 | |
| B. | 红葡萄酒营养丰富(含葡萄糖、维生素C等),常添加微量的二氧化硫,利用二氧化硫还原性,防止红葡萄酒中某营养成分被氧化 | |
| C. | 某雨水放置一段时间后pH由4.68变为4.28,因为水中亚硫酸被空气中氧气氧化成硫酸 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
17.在25℃时,某氯化铵溶液的pH=4,下列说法中不正确的是( )
| A. | 溶液中c(H+)>c(OH-),且Kw=c(H+).c(OH-)=1×10-14mol2/L2 | |
| B. | 由水电离出来的H+浓度为1×10-14mol/L-1 | |
| C. | 溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 此溶液中由水电离出来的c(H+)=c(OH-) |
14.下列实验中,所选装置不合理的是( )


| A. | 分离Na2CO3溶液和CH3COOC2H5,选④ | B. | 用CCl4提取碘水中的碘,选③ | ||
| C. | 用溴水除去甲烷中混有的乙烯,选⑤ | D. | 粗盐提纯,选①和② |
11.下列有关SO2的性质的探究实验报告记录的实验现象正确的是( )
| 实验 | 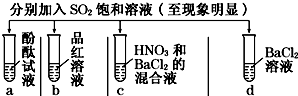 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色溶液 | |
| C | 无色 | 无色 | 白色沉淀 | 无色溶液 | |
| D | 无色 | 无色 | 无色沉淀 | 无色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
12.已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O3(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O3(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0,△H3<0 | B. | △H1>△H2 | C. | △H1=△H2+△H3 | D. | △H3=△H4+△H5 |