题目内容
12.下列物质中属于有机物的是( )| A. | 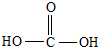 | B. | NH4SCN | C. | 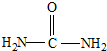 | D. | 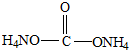 |
分析 根据有机物一般是指含碳的化合物,无机物一般是指不含碳的化合物,但碳的氧化物、碳酸、碳酸盐等性质与无机物相似,常归为无机物.
解答 解:A、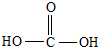 是碳酸,不属于有机物.故A错误;
是碳酸,不属于有机物.故A错误;
B、NH4SCN属于铵盐,不属于有机物,故B错误;
C、尿素CO(NH2)2中含有氮元素,属于氮肥,其中含有碳元素,属于有机物,故C正确;
D、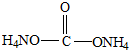 属于铵盐,不属于有机物,故D错误.
属于铵盐,不属于有机物,故D错误.
故选C.
点评 该题是基础性试题的考查,难度不大.该题的关键是明确有机物和无机物的区别,然后灵活运用即可,有利于培养学生的逻辑思维能力和发散思维能力.

练习册系列答案
相关题目
2.下列物质在水中的电离方程式书写正确是( )
| A. | NaHSO4═Na++HSO4- | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2CO3?2H++CO32- | D. | A12(SO4)3═2A13++3SO42- |
20.下列叙述中,肯定能说明金属甲比金属乙金属性强的是( )
| A. | 甲原子最外层电子数比乙原子最外层电子数少 | |
| B. | 甲原子电子层数比乙原子电子层数多 | |
| C. | 1mol甲从酸中置换生成的氢气比1mol乙从酸中置换生成的氢气多 | |
| D. | 常温下,甲能与水反应生成氢气,而乙不能 |
4.含6.02×1023个中子的${\;}_3^7Li$的质量是( )
| A. | $\frac{7}{4}g$ | B. | 4.7 g | C. | 7.4 g | D. | $\frac{4}{7}g$ |
2.下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
(1)活性炭(2)氯水(3)二氧化硫(4)臭氧 (5)过氧化钠 (6)双氧水.
(1)活性炭(2)氯水(3)二氧化硫(4)臭氧 (5)过氧化钠 (6)双氧水.
| A. | (1)(2)(4)(6) | B. | (1)(2)(3)(5) | C. | (2)(4)(5)(6) | D. | (3)(4)(5)(6) |
 .
.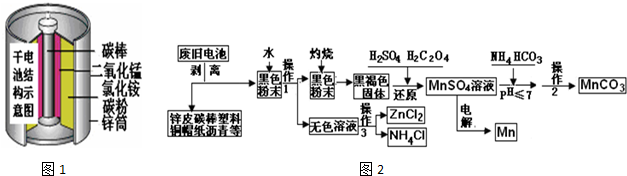
 如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物,F为磁性物质.它们存在如下转化关系,反应中生成的水及次要产物均已略去.
如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物,F为磁性物质.它们存在如下转化关系,反应中生成的水及次要产物均已略去.