题目内容
17.利用如图所示装置可以将温室气体CO2转化为燃料气体CO.下列说法中,正确的是( )
| A. | 该过程是将太阳能转化为化学能的过程 | |
| B. | 电极a表面发生还原反应 | |
| C. | 该装置工作时,H+从b极区向a极区移动 | |
| D. | 该装置中每生成1 mol CO,同时生成1 mol O2 |
分析 该装置中,根据电子流向知,a是负极,b是正极,负极反应式为2H2O-4e-=4H++O2↑,正极反应式为CO2+2e-+2H+=CO+H2O,电解质溶液中阳离子向正极移动,据此分析解答.
解答 解:A.根据图知,该装置中有太阳能转化为化学能、化学能转化为电能,故A正确;
B.根据电子流向知,a是负极,发生氧化反应,故B错误;
C.电解质溶液中阳离子向正极移动,所以H+从a极区向b极区移动,故C错误;
D.a是负极,b是正极,负极反应式为2H2O-4e-=4H++O2↑,正极反应式为CO2+2e-+2H+=CO+H2O,则根据得失电子守恒,每生成1 mol CO,同时生成0.5mol O2,故D错误;
故选A.
点评 本题考查化学电源新型电池,明确原电池原理、电极反应等即可解答,难点是电极反应式的书写,题目难度中等,侧重于考查学生对原电池原理的应用能力.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案
相关题目
18.下列说法正确的是( )
| A. | 氯气通入水中,有化学键的断裂与形成 | |
| B. | MgCl2晶体中存在离子键与共价键 | |
| C. | NH3和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | CO2和SiO2晶体都是由分子构成的 |
8.标准状况下有如下气体:①6.72LCH4②3.01×1023个HCl分子 ③13.6gH2S ④0.2molNH3下列对这四种气体的关系排列的组合中正确的是( )
| A. | 体积:②>③ | B. | 密度:④>① | C. | 质量:③>① | D. | 氢原子个数:①>② |
2. 电解质溶液的电导率越大,导电能力越强.用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是( )
 电解质溶液的电导率越大,导电能力越强.用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是( )
电解质溶液的电导率越大,导电能力越强.用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是( )| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A、C两点对应溶液均呈中性 | |
| C. | B点溶液中:c(Na+)>c(OH-)>c(CH3COO-) | |
| D. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L |
9.下列说法中,符合ⅦA族元素结构与性质特征的是( )
| A. | 原子易形成-2价阴离子 | |
| B. | 单质均为双原子分子,具有氧化性 | |
| C. | 原子半径随原子序数递增逐渐减小 | |
| D. | 氢化物的稳定性随原子序数递增依次增强 |
6.有M、N、P、E四种金属,①M+N2+=N+M2+;②M、P用导线连接放入稀盐酸中,M表面有大量气泡;③电解过程中,阴极存在N2+和E2+两种离子时,E2+优先放电.则四种金属的活动性由强到弱的顺序为( )
| A. | E、N、M、P | B. | M、N、P、E | C. | P、M、N、E | D. | P、N、M、E |
7.下列说法正确的是( )
| A. | 用试管夹夹试管应从试管底往上套,拇指按在试管夹的短柄上 | |
| B. | 装碘的试剂瓶中残留的碘可以用酒精洗涤 | |
| C. | 配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用滴管滴加蒸馏水到刻度线 | |
| D. | 定容时,俯视刻度线,会使所配溶液的浓度偏低 |
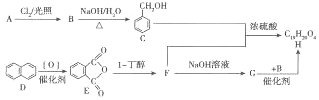
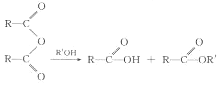 ②反应F→G仅发生中和反应
②反应F→G仅发生中和反应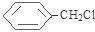 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$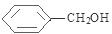 +NaCl.
+NaCl.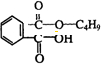 .
.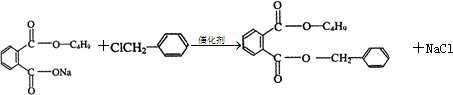 .
.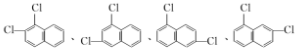 中任一种(写出一种即可).
中任一种(写出一种即可).