��Ŀ����
13���״���CH3OH����һ�ֻ����л�����ԭ�Ϻ�����ȼ�ϣ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ��������ºϳɼ״�������Ӧ���£���CO��g��+2H2��g��?CH3OH��g����H1=-99kJ•mol-1
��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H2
��CO2��g��+H2��g��?CO��g��+H2O��g����H3=+41kJ•mol-1
����Ӧ�У�2CH3OH��g��?CH3OCH3��g��+H2O��g�� ��
��1���״������и�ԭ�Ӱ뾶�Ӵ�С��˳��Ϊr��C������O����r��H����
��2����H2=-58kJ•mol-1
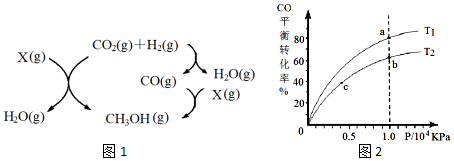
��3���������ϳɼ״��ķ�Ӧ��Ƴ���ͼ1��ʾ������;��������XΪ2H2��
��4��������Ӧ�ٽ���ʵ��̽����
��CO��H2Ͷ�ϱ�Ϊ1��2ʱ�����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ2��ʾ��
��ͼ�ж�Ӧ���ƽ�ⳣ��Ka��Kb��Kc��С��ϵΪKa��Kb=Kc��
�ڷ�Ӧ�ں��¡������½��У�����˵��������Ϊ�жϷ�Ӧ�ﵽƽ��״̬����BC�����ţ���
A�����������ܶȲ���
B����Ӧ����������ѹǿ���ٱ仯
C����������ƽ����Է�����������
D������CH3OH����������H2���ʵ�2��
�۽�l molCO��2molH2ͨ��1L�ܱ������У���300���£��ﵽƽ��ʱCO��ת����Ϊ90%����ƽ�ⳣ��KΪ225��
��5����̽������Ӧ�ٹ����з������ϳ���ֻ��CO��H2������ܳ�������״����
�ٻ��н϶�ĸ���ƷCH3OCH3����
���γɻ�̼���л���̼�����Ǵ������棩
������������CO2����ɼ�������״�����Խ���
��CO2��H2��Ӧ����H2O������CH3OCH3������
��C+CO2$\frac{\underline{\;\;��\;\;}}{\;}$2CO���û�ѧ����ʽ��ʾ��
���� ��1�����ݵ��Ӳ���Խ��뾶Խ���Ӳ�����ͬʱ�˵����Խ��뾶ԽС������ԭ�Ӱ뾶��С��
��2�����ݸ�˹���ɷ�����
��3����CO+X=CH3OH�����������غ�������
��4����CO��g��+2H2��g��?CH3OH��g����H1=-99kJ•mol-1����Ӧ�Ƿ��ȷ�Ӧ�������¶�Խ��CO��ƽ��ת����ԽС����T2��T1����ƽ�ⳣ�����¶ȵĺ�����
��A�����������ܶ�һֱ���䣻
B����Ӧ����������ѹǿ���ٱ仯��˵����������ʵ������䣻
C����������ƽ����Է����������䣬˵����������ʵ������䣻
D������CH3OH����������H2���ʵ�2��������˵�����ʲ��䣻
�۸�������ʽ���ƽ�ⳣ������ʽ�������
��5���ٷ�ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g������ˮ�Ը���Ӧ2CH3OH��g��?CH3OCH3��g��+H2O��g�����������ã����Ի��н϶�ĸ���ƷCH3OCH3���ɣ��ɴ˷������
���γɻ�̼��������������CO2������һ����̼���壻
��� �⣺��1�����ݵ��Ӳ���Խ��뾶Խ���Ӳ�����ͬʱ�˵����Խ��뾶ԽС�����Լ״������и�ԭ�Ӱ뾶�Ӵ�С��˳��Ϊr��C������O����r��H�����ʴ�Ϊ��r��C������O����r��H����
��2����֪��CO��g��+2H2��g��?CH3OH��g����H1=-99kJ•mol-1����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H2����CO2��g��+H2��g��?CO��g��+H2O��g����H3=+41kJ•mol-1�����ݸ�˹���ɡ�H2=��H1+��H3=-58kJ•mol-1���ʴ�Ϊ��-58kJ•mol-1��
��3����CO+X=CH3OH�����������غ��֪X��2H2���ʴ�Ϊ��2H2��
��4����CO��g��+2H2��g��?CH3OH��g����H1=-99kJ•mol-1����Ӧ�Ƿ��ȷ�Ӧ�������¶�Խ��CO��ƽ��ת����ԽС����T2��T1����ƽ�ⳣ�����¶ȵĺ���������ƽ�ⳣ��Ka��Kb��Kc��С��ϵΪKa��Kb=Kc���ʴ�Ϊ��Ka��Kb=Kc��
��A�����������ܶ�һֱ���䣬���Բ���˵����ƽ��״̬���ʴ���
B����Ӧ����������ѹǿ���ٱ仯��˵����������ʵ������䣬��ƽ��״̬������ȷ��
C����������ƽ����Է����������䣬˵����������ʵ������䣬��ƽ��״̬������ȷ��
D������CH3OH����������H2���ʵ�2��������˵�����ʲ��䣬���Բ���˵����ƽ��״̬���ʴ���
��ѡ��BC��
�۽�l molCO��2molH2ͨ��1L�ܱ������У���300���£��ﵽƽ��ʱCO��ת����Ϊ90%��
CO��g��+2H2��g��?CH3OH��g��
c������ 1 2 0
c���䣩 0.9 1.8 0.9
c��ƽ�� 0.1 0.2 0.9
����K=$\frac{0.9}{0.1��0��{2}^{2}}$=225���ʴ�Ϊ��225��
��5���ٷ�ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g������ˮ�Ը���Ӧ2CH3OH��g��?CH3OCH3��g��+H2O��g�����������ã����Ի��н϶�ĸ���ƷCH3OCH3���ɣ��ʴ�Ϊ��CO2��H2��Ӧ����H2O������CH3OCH3�����ɣ�
���γɻ�̼��������������CO2������һ����̼���壬���Է�Ӧ�Ļ�ѧ����ʽΪ��C+CO2$\frac{\underline{\;\;��\;\;}}{\;}$2CO���ʴ�Ϊ��C+CO2$\frac{\underline{\;\;��\;\;}}{\;}$2CO��
���� ���⿼���֪ʶ��϶࣬��Ŀ�ۺ��Խ�ǿ���ѶȽϴ���Ҫ�����˻�ѧƽ�ⳣ����С �ıȽϡ���˹���ɵ�Ӧ�á���ѧƽ����йؼ��㣬��һ�����Ѷȣ�

| A�� | ��֪2H2��g��+O2��g���T2H2O��g����H=-483.6 kJ•mol-1����������ȼ����Ϊ241.8 kJ•mol-1 | |
| B�� | ��֪NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.3 kJ•mol-1����40.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�������С��57.3 kJ | |
| C�� | ��֪2C��s��+2O2��g���T2CO2��g����H=a��2C��s��+O2��g���T2CO��g����H=b����a��b | |
| D�� | ��֪CH4��g��+H2O��g���TCO��g��+3 H2��g����H=+206.1 kJ•mol-1����Ӧ������ʹ�ô�������H��С |
| A�� | ��ɫ��Һ�п��ܴ�������Al3+��NH4+��Cl-��HS- | |
| B�� | ������Һ�п��ܴ�������Na+��ClO-��SO42-��I- | |
| C�� | ��������Һ�п��ܴ�������Na+��K+��Cl-��HCO3- | |
| D�� | ������Һ�п��ܴ�������Fe3+��K+��SCN-��SO42- |
| A�� | �Թ� | B�� | ����ƿ | C�� | ������ | D�� | Բ����ƿ |

��֪��i����ϴ���ƹ�����õ��������Ҫ�ɷ������ʾ��
| �ɷ� | Cl- | ����HCl | Fe2+ | Fe3+ |
| ����g•/L-1 | 130-160 | 50-70 | 60-80 | 0 |
��1����ϴ���ƹ���ʱ������Ӧ�����ӷ���ʽ��2H++FeO=Fe2++H2O��6H++Fe2O3•H2O+Fe�T3Fe2++4H2O��
��2������II�У���������Ҫ��Ӧ��FeCl2��s��ʮH2SO4��aq��?FeSO4��s��+2HCl�� aq����
�ټ������H2SO4������������Fe2+ˮ�⣺��ֹpH��4ʱ��Fe2+������������ͬʱ�ṩH+����HC1������ݳ����ṩSO42-����FeSO4��������������д�����㣩��
���û�ѧƽ��ԭ�������������Ŀ�ģ���������HCl���壬�ٽ�ƽ��FeCl2��s��+H 2SO4��aq��?FeSO4��s��+2HCl��aq��������Ӧ�����ƶ���������FeSO4�����������
��3������III�У�FeSO4�����������յõ���β���к������ֿ��������������������˹��̷�����Ӧ�Ļ�ѧ����ʽ��2FeSO4$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3����
��4������IV������Ӧ�����ӷ���ʽ��2Fe2++H2O2+8Cl-+2H+�T2FeCl4-+2H2O��
��5������V�������ӽ�����֬�ɽ�FeCl4-ѡ�����������룬����̿ɱ�ʾΪROH+X- $?_{�Ѹ�}^{����}$RX+OH-������֬�������ͺ��ֱ����ˮϴ����֬�����Ѹ���ͬʱ�Ѹ����̷�����Ӧ��FeCl4-?Fe3++4C1-��
����������Һ�����½���ԭ�������������ڿջ���֬��������ʱ����֬�ϵ�OH-����������������������Һ��
��ϴ��Һ����Ҫ���е�������FeCl3��HC1��
| ��Ӧ | �����̵� N2��g��+O2��g��?2NO��g�� | ��ҵ�̵� N2��g��+3H2��g��?2NH3��g�� | |||
| �¶�/�� | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84��10-31 | 0.1 | 5��10-8 | 2��104 | 7��103 |
����һ���¶��£���һ�����N2��O2ͨ�뵽���Ϊ1L���ܱ������У����������̵�����Ӧ�ﵽƽ��ı�������������ʹƽ��������Ӧ�����ƶ���ƽ�ⳣ���������b��
a������ѹǿ b������Ӧ���Ũ�� c��ʹ�ô��� d�������¶�
�۴ӷ��ӽṹ�ǶȽ��͡������̵����͡���ҵ�̵�����Ӧ�Ļ�ܶ��ܸߵ�ԭ����������N��N���ܴܺϿ�N��N��Ҫ���սϸ�������
��2�������������ݿ�֪�������̵����ķ�Ӧ������еij̶�С�����ʺϴ��ģ��������������������úϳɰ��ķ������й�ҵ�̵���
�ٴ�ƽ���ƶ��Ƕȿ��ǣ���ҵ�̵�Ӧ��ѡ������������ʵ�ʹ�ҵ����ȴѡ��500�����ҵĸ��£�������ԭ��ӷ�Ӧ���ʽǶȿ��ǣ����¸��ã����Ӵ������Ե��ۺ����ؿ���ѡ��500�����Һ��ʣ�
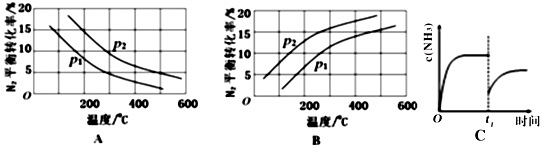
�ڽ�0.1molN2��0.1molH2ͨ��һ�ݻ��ɱ�������н��й�ҵ�̵���Ӧ������ͼ��ʾN2��ƽ��ת�����ڲ�ͬѹǿ��P1��P2�������¶ȱ仯��������ȷ����A���A����B�������Ƚ�P1��P2�Ĵ�С��ϵ ��2����1����300�桢ѹǿP2ʱ�ﵽƽ�⣬�����ݻ�ǡΪ100L�����״̬�·�Ӧ��ƽ�ⳣ��K=1.3��l05 ������������2λ��Ч���֣���
�ۺϳɰ���Ӧ�ﵽƽ���t1ʱ�̵���Ũ��������ͼC�仯�ɲ�ȡ�Ĵ�ʩ�������ݻ����������������������������Ͱ�����Ũ�ȣ�
��3��������꣬���п�ѧ������ڳ��¡���ѹ�������������ºϳɰ�������˼·��
��Ӧԭ��Ϊ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g�������䷴Ӧ�ȡ�H=+1530 kJ•mol-1��
����֪��
N2��g��+3H2��g��?2NH3��g����H1=-92.4kJ•mol-1
2H2��g��+O2��g��?2H2O��l����H2=-571.6kJ•mol-1 ��
�ٽ�����Ͷ�뵽FeCl3��Һ
�ڹ���NaOH��Һ��������Һ
��Na2O2Ͷ��FeCl2��Һ��
| A�� | �� | B�� | �� | C�� | �ڢ� | D�� | �٢� |
| A�� | ǿ�ᡢǿ����������ǿ����ʣ����ᡢ�����ˮ��������� | |
| B�� | �������Һ�����Ե�ǿ������λ�����Һ�������ƶ������Ӷ����й� | |
| C�� | ����ǿ���Թ��ۼ��Ļ�����һ����ǿ����� | |
| D�� | ��������ǿ����ʣ�̼������Ҳ��ǿ����� |