题目内容
HO2(超氧酸)是一种弱酸,具有极高的活性,一定条件下,铜与盐酸,氧气发生如下反应可生成HO2:Cu+HCl+O2=CuCl+HO2,下列说法正确的是( )
| A、上述反应中,O2发生了氧化反应 |
| B、若1molO2参加反应,电子转移的物质的量是2mol |
| C、上述反应中,HO2是还原产物 |
| D、上述反应的离子方程式为:Cu+Cl-+O2=CuCl+O2- |
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应Cu+HCl+O2=CuCl+HO2中Cu元素化合价升高,被氧化,O元素化合价降低,被还原,O2为氧化剂,结合元素化合价的变化解答该题.
解答:
解:A.反应中O元素化合价降低,被还原,发生还原反应,故A错误;
B.反应中2molO原子失去1mol电子,则1molO2参加反应,电子转移的物质的量是1mol,故B错误;
C.O元素化合价降低,被还原,HO2为还原产物,故C正确;
D.HO2是一种弱酸,应写成化学式,其反应的离子方程式为Cu+H++Cl-+O2=CuCl+HO2,故D错误.
故选C.
B.反应中2molO原子失去1mol电子,则1molO2参加反应,电子转移的物质的量是1mol,故B错误;
C.O元素化合价降低,被还原,HO2为还原产物,故C正确;
D.HO2是一种弱酸,应写成化学式,其反应的离子方程式为Cu+H++Cl-+O2=CuCl+HO2,故D错误.
故选C.
点评:本题考查氧化还原反应,题目难度不大,注意把握元素化合价的变化,为解答该题的关键,易错点为D,注意把握题给信息.

练习册系列答案
相关题目
某阳离子M2+共有10个电子,其质量数为24,那么它核内的中子数为( )
| A、10 | B、12 | C、14 | D、16 |
如图表示三种原子的原子结构: 其中
其中 表示质子或电子,
表示质子或电子, 表示中子,则下列有关①②③的叙述正确的组合是( )
表示中子,则下列有关①②③的叙述正确的组合是( )
a、①②③互为同位素
b、①②③互为同素异形体
c、①②③是三种化学性质不同的粒子
d、①②③具有相同的质量数
e、①②③具有相同的质量
f、①②③是三种不同的核素.
 其中
其中 表示质子或电子,
表示质子或电子, 表示中子,则下列有关①②③的叙述正确的组合是( )
表示中子,则下列有关①②③的叙述正确的组合是( )a、①②③互为同位素
b、①②③互为同素异形体
c、①②③是三种化学性质不同的粒子
d、①②③具有相同的质量数
e、①②③具有相同的质量
f、①②③是三种不同的核素.
| A、a f |
| B、b c |
| C、d e |
| D、e f |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法错误的是( )
| A、使用催化剂是为了加快反应速率,提高生产效率 |
| B、在上述条件下,SO2不可能100%地转化为SO3 |
| C、为了提高SO2的转化率,应适当提高O2的浓度 |
| D、达到平衡时,SO2的浓度与SO3的浓度相等 |
下列化合物中,既能发生消去反应,又能发生水解反应的是( )
| A、氯仿 | B、一氯甲烷 |
| C、乙醇 | D、氯乙烷 |
下列关于苯乙烯(结构简式为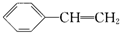 )的叙述,错误的是( )
)的叙述,错误的是( )
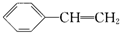 )的叙述,错误的是( )
)的叙述,错误的是( )| A、可以和溴水反应 |
| B、是乙烯的同系物 |
| C、化学式为C8H8 |
| D、1 mol苯乙烯最多可以和4 mol H2发生加成反应 |
下列说法错误的是( )
| A、分子组成为C4H100的醇有4种 |
| B、1 mol二氯乙烷与Cl2发生取代反应,反应完全共需4 mol Cl2 |
| C、(CH3)3CCH2CH3的一氯代物有3种 |
| D、乙烷与Cl2反应与乙烯与C12的反应类型相同 |
 美国每日科学网站文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分-“表没食子儿茶素没食子酸酯”(EGCG).研究显示,该成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.已知EGCG的结构简式如图,有关EGCG的说法不正确的是( )
美国每日科学网站文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分-“表没食子儿茶素没食子酸酯”(EGCG).研究显示,该成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.已知EGCG的结构简式如图,有关EGCG的说法不正确的是( )| A、EGCG分子中含有两个手性碳原子 |
| B、EGCG遇FeCl3溶液能发生显色反应 |
| C、EGCG在空气中不易被氧化 |
| D、EGCG可与氢氧化钠溶液反应 |
下列表示物质结构的化学用语正确的是( )
A、NaCl的电子式: |
B、N2的电子式: |
C、HF的电子式: |
D、F-离子结构示意图: |