题目内容
NO2通过盛有水的洗气瓶,转移0.02mol电子时,参加反应的NO2气体在标准状况下的体积为( )
| A、224mL |
| B、336mL |
| C、448mL |
| D、672mL |
考点:氮的氧化物的性质及其对环境的影响
专题:氮族元素
分析:根据反应4NO2+2H2O+O2═4HNO3,结合氮元素的化合价变化以及电子转移的知识来判断.
解答:
解:NO2通过盛有水的洗气瓶,发生反应4NO2+2H2O+O2═4HNO3,消耗4mol二氧化氮气体,转移电子是4mol,当转移0.02mol电子时,参加反应的NO2气体时0.02mol,体积是448mL.
故选C.
故选C.
点评:本题考查学生二氧化氮的性质,注意知识的整理记忆是关键,难度不大.

练习册系列答案
相关题目
H+浓度相同的两种一元酸HX和HY溶液,分别取100mL加入足量的镁粉,充分反应后,收集到H2的体积分别为V(HX)和V(HY),在相同条件下,V(HX)>V(HY),则下列说法正确的是( )
| A、HX可能是强酸 |
| B、HY一定是强酸 |
| C、HX的酸性强于HY的酸性 |
| D、反应开始时二者生成氢气的速率相同 |
下列物质中,不属于糖类的是( )
| A、麦芽糖 | B、淀粉 |
| C、蛋白质 | D、蔗糖 |
某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g)△H<0.下图表示该反应的速率(υ)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )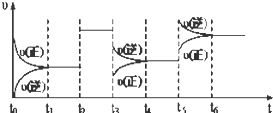

| A、t3时降低了温度 |
| B、t5时增大了压强 |
| C、t2时加入了催化剂 |
| D、t4~t5时间内转化率一定最低 |
运用相关化学知识进行判断,下列结论正确的是( )
| A、晶体硅熔点高硬度大,因而可用于制作半导体材料 |
| B、SO2使溴水褪色与乙醛使溴水褪色的原理相同 |
| C、硅胶可作袋装食品的干燥剂,P2O5可用于干燥Cl2和NH3 |
| D、金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 |
对于H-+H2O═H2+OH-说法正确的是( )
| A、该反应属于置换反应 |
| B、若该反应中有1mol电子转移,则生成H2是22.4L |
| C、水是氧化剂 |
| D、H2只是氧化产物 |
1gH2燃烧生成液态水放出142.9kJ的热量,下列热化学方程式书写正确的是( )
| A、2H2(g)+O 2(g)=2H2O (1),△H=-142.9 kJ?mol-1 | ||
| B、2H2(g)+O 2(g)=2H2O (1),△H=-571.6 kJ?mol-1 | ||
| C、2H2+O2=2H2O,△H=-571.6kJ?mol-1 | ||
D、H2(g)+
|
下列图式表示正确的是( )
A、二氧化碳 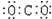 |
B、N原子的价电子电子排布图: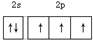 |
C、铝离子的结构示意图 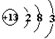 |
| D、乙醇的分子式:C2H5OH |