题目内容
1.下列关于丙烯(CH3-CH=CH2)的说法正确的( )| A. | 丙烯分子有8个σ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp3杂化 | |
| C. | 丙烯分子不存在非极性键 | |
| D. | 丙烯分子中3个碳原子不在同一直线 |
分析 A.单键为σ键,双键含有1个σ键、1个π键;
B.丙烯中不饱和碳原子形成3个σ键,没有孤电子对,杂化轨道数目为3;
C.碳原子之间形成非极性键;
D.不饱和碳原子连接的原子形成平面三角形结构.
解答 解:A.单键为σ键,双键含有1个σ键、1个π键,丙烯(CH3-CH=CH2)分子中有8个σ键,1个π键,故正确;
B.丙烯中甲基中碳原子形成4个σ键,没有孤电子对,杂化轨道数目为4,采取sp3杂化,而不饱和碳原子形成3个σ键,没有孤电子对,杂化轨道数目为3,采取sp2杂化,故B错误;
C.C原子与H原子之间形成极性键,而碳原子之间形成非极性键,故C错误;
D.不饱和碳原子连接的原子形成平面三角形结构,故丙烯分子中3个碳原子不在同一直线,故D正确,
故选:AD.
点评 本题考查化学键、杂化方式判断、分子空间结构等,注意理解掌握杂化方式判断.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
12.下列关于碳酸钠和碳酸氢钠的叙述,正确的是( )
| A. | 常温时,在水中的溶解性:碳酸钠>碳酸氢钠 | |
| B. | 热稳定性:碳酸钠<碳酸氢钠 | |
| C. | 质量相同时,分别与同体积同浓度盐酸反应的快慢:碳酸钠>碳酸氢钠 | |
| D. | 物质的量相同时,分别与足量的盐酸反应,生成CO2的质量:碳酸钠<碳酸氢钠 |
16.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如下:
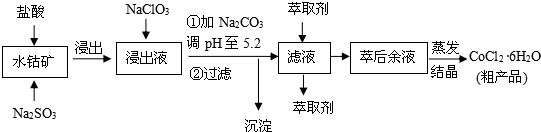
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH表:(金属离子浓度为:0,01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH表:(金属离子浓度为:0,01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
6.下列叙述中不正确的是( )
| A. | Na2O2是淡黄色固体,Na2O 是白色固体,二者都能与水反应生成 NaOH | |
| B. | Na和O2在加热时反应生成 Na2O2,在常温下反应生成 Na2O | |
| C. | Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2 | |
| D. | 2 g H2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g |
13.下列说法正确的是( )
| A. | 钠钾合金比纯钠的熔点高 | |
| B. | 鉴别碳酸氢钠中含有纯碱的方法是加热看是否有气体生成 | |
| C. | Fe2O3可以用作红色油漆或涂料 | |
| D. | Cl2具有漂白性 |
10.下列关于乙烯的说法不正确的是( )
| A. | 是无色液体 | |
| B. | 可做水果催熟剂 | |
| C. | 能使KMnO4酸性溶液褪色 | |
| D. | 能跟溴的四氯化碳溶液发生加成反应 |
11.下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:1的是( )
| A. | 对二甲苯 | B. | 2-丙醇 | C. | 2-甲基丙烯 | D. | 均三甲苯 |