题目内容
关于CH3COONa与CH3COOH的混合溶液,下列说法不正确的是( )
| pH | 离子浓度关系 | |
| A | pH<7 | c(CH3COO-)>c(Na+) |
| B | pH>7 | c(CH3COO-)<c(Na+) |
| C | pH=7 | c(CH3COO-)=c(Na+) |
| D | pH<7 | c(CH3COO-)<c(Na+) |
| A、A | B、B | C、C | D、D |
考点:离子浓度大小的比较
专题:
分析:常温下,CH3COONa与CH3COOH的混合溶液中,若混合液的pH<7,则c(OH?)<c(H+),若pH=7,则c(OH?)=c(H+),若pH>7,则c(OH?)>c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)判断c(CH3COO?)、c(Na+)相对大小.
解答:
解:A.常温下,CH3COONa与CH3COOH的混合溶液的pH<7,则:c(OH?)<c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)>c(Na+),故A正确;
B.混合液的pH>7,则c(OH?)>c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)<c(Na+),故B正确;
C.混合液的pH=7,则:c(OH?)=c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)=c(Na+),故C正确;
D.混合液的pH<7,则:c(OH?)<c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)>c(Na+),故D错误;
故选D.
B.混合液的pH>7,则c(OH?)>c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)<c(Na+),故B正确;
C.混合液的pH=7,则:c(OH?)=c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)=c(Na+),故C正确;
D.混合液的pH<7,则:c(OH?)<c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)>c(Na+),故D错误;
故选D.
点评:本题考查混合液中离子浓度大小比较,题目难度中等,根据pH大小确定c(OH?)、c(H+)相对大小,再结合电荷守恒判断即可,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有机物不能通过加成反应制取的是( )
| A、CH3CH2Cl |
| B、CH2Cl-CH2Cl |
| C、CH3-CH2OH |
| D、CH3-COOH |
在3Cu2S+22HNO3=6Cu(NO3)2+10NO↑+3H2SO4+8H2O的反应中,转移电子的总数为( )
| A、12 | B、22 | C、24 | D、30 |
下列操作不能用于检验NH3的是( )
| A、气体使湿润的酚酞试液变红 |
| B、气体能使湿润的红色石蕊试纸变蓝 |
| C、气体与蘸有浓H2SO4的玻璃棒靠近 |
| D、气体与蘸有浓盐酸的玻璃棒靠近 |
下列溶液中,溶质的物质的量浓度为1mol/L的是( )
| A、含Na+为2mol的Na2SO4溶液 |
| B、将31g Na2O溶于水并配成1L的溶液 |
| C、将0.5mol/L的KNO3溶液100mL加热蒸发掉50g水的溶液 |
| D、将58.5gNaCl溶于1L水所得的溶液 |
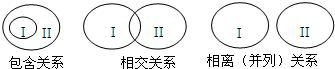 大多数概念间存在如图三种关系:
大多数概念间存在如图三种关系: