题目内容
14.化学与生活密切相关,下列说法不正确的是( )| A. | 在汽车排气管上加装“催化转化器”可以减少有害气体的排放 | |
| B. | “84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感 | |
| C. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物“,PM2.5在空气中有可能形成胶体 | |
| D. | 碳酸钡、碳酸氢钠、氢氧化铝均可作为抗胃酸药物使用 |
分析 A.在汽车排气管上加装“催化转化器”使一氧化碳和一氧化氮进行转化为无毒气体;
B.“84”消毒液,其主要成分是NaClO,具有强氧化性,能作消毒剂;
C.小于0.1微米(1微米=1000纳米)的颗粒称为浮尘,浮尘与空气形成的分散系属于胶体;
D.胃酸的成分为盐酸,治疗胃酸过多需根据药物的成分及与酸的反应来分析.
解答 解:A.在汽车排气管上加装“催化转化器”使一氧化碳和一氧化氮进行转化为无毒气体,减少有害气体的排放,故A正确;
B.体的排放,故A正确;
B.“84”消毒液的主要成分是NaClO,具有强氧化性,能作消毒剂从而预防流感,故B正确;
C.④“PM2.5”是指直径小于等于2.5微米的颗粒物,其中小于0.1微米(1微米=1000纳米)的颗粒称为浮尘,浮尘与空气形成的分散系属于胶体,故C正确;
D.胃酸的主要成分为盐酸,胃酸与碳酸氢钠反应生成氯化钠和二氧化碳气体,反应的离子方程式为HCO3-+H+=CO2↑+H2O,胃酸与氢氧化铝反应生成氯化铝和水,反应的离子方程式为Al(OH)3+3H+=Al3++3H2O,碳酸氢钠和氢氧化铝可用来治疗胃酸过多,碳酸钡能与胃液中的盐酸反应生成可溶性的氯化钡而导致中毒,反应的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,故D错误;
故选:D.
点评 本题考查化学与生活、生产密切相关的知识,学习中注意常见有机物、抗酸药物使用的原理、PM2.5,题目难度不大.

练习册系列答案
相关题目
5.相对分子质量均为88的饱和一元醇和饱和一元羧酸发生酯化反应,生成酯的结构可能有(不考虑立体异构)( )
| A. | 8种 | B. | 12种 | C. | 16种 | D. | 32种 |
2.某兴趣小组进行铁矿石中含铁量的测定,实验过程如图:

下列说法正确的是( )

下列说法正确的是( )
| A. | 加热煮沸的主要目的是除去溶液中溶解的氧气 | |
| B. | 稀释过程中用到的玻璃仪器主要有烧杯、玻璃棒、胶头滴管 | |
| C. | 滴定过程中可用淀粉溶液作指示剂 | |
| D. | 铁矿石中铁的质量分数为70% |
9.下列物质中既有离子键又有共价键的是 ( )
| A. | MgO | B. | NaOH | C. | CaCl2 | D. | CO2 |
19.丁烷的一氯代物共有多少种( )
| A. | 3 | B. | 5 | C. | 4 | D. | 2 |
4. 元素周期表前四周期的五种元素R、X、T、Z、Q在周期表中的相对位置如图所示,其中T单质在常温下为气态,Q单质在常温下为液态,则下列判断正确的是( )
元素周期表前四周期的五种元素R、X、T、Z、Q在周期表中的相对位置如图所示,其中T单质在常温下为气态,Q单质在常温下为液态,则下列判断正确的是( )
 元素周期表前四周期的五种元素R、X、T、Z、Q在周期表中的相对位置如图所示,其中T单质在常温下为气态,Q单质在常温下为液态,则下列判断正确的是( )
元素周期表前四周期的五种元素R、X、T、Z、Q在周期表中的相对位置如图所示,其中T单质在常温下为气态,Q单质在常温下为液态,则下列判断正确的是( )| A. | 原子半径及离子半径:X>T | |
| B. | R、T、Q的氢化物的热稳定性和还原性均依次减弱 | |
| C. | 相同物质的量的T、Z的单质的质量中Z的大 | |
| D. | T的非金属性比X的非金属性强,因此T的含氧酸的酸性比X的含氧酸的酸性强 |
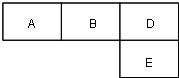 M、A、B、D、N、E五种短周期元素的原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在如图(周期表的一部分)占有相应的位置,它们的原子序数之和为37.
M、A、B、D、N、E五种短周期元素的原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在如图(周期表的一部分)占有相应的位置,它们的原子序数之和为37.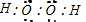 .
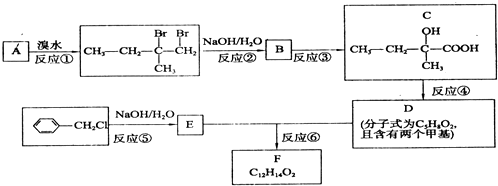
.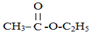 相关物质间转化关系如图:
相关物质间转化关系如图: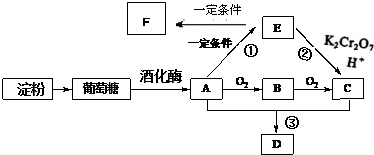
 +CH2CH2OH$?_{△}^{浓硫酸}$
+CH2CH2OH$?_{△}^{浓硫酸}$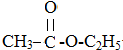 +H2O
+H2O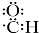

 .
. .
. .
.
 .
.