题目内容
Fe和Al是两种常见的金属,将它们按一定的质量比组成混合物.取m克该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为a L,则反应的离子方程式为 ;混合物中的Fe的质量为 (用含字母的数学式表示).
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:铁和氢氧化钠不反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,根据氢气和铝之间的关系式计算n(Al)及m(Al),铁的质量为mg-m(Al).
解答:
解:铁和氢氧化钠不反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,n(H2)=
=
mol,由2Al~3H2↑,n(Al)=
×
mol=
mol,m(Al)=
mol×27g/mol=
g,则铁的质量为mg-
g=(m-
)g,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(m-
)g.
| aL |
| 22.4L/mol |
| a |
| 22.4 |
| 2 |
| 3 |
| a |
| 22.4 |
| 5a |
| 168 |
| 5a |
| 168 |
| 45a |
| 56 |
| 45a |
| 56 |
| 45a |
| 56 |
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;(m-
| 45a |
| 56 |
点评:本题考查化合物的有关计算、离子方程式的书写,注意铝和氢氧化钠溶液的反应中水参加反应,为易错点.

练习册系列答案
相关题目
下列除去杂质的方法正确的是( )
| A、除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离 |
| B、除去溴苯中少量的溴,可用苯进行洗涤、分液 |
| C、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液,然后干燥、蒸馏 |
| D、除去氯气中少量的氯化氢,通过NaOH溶液进行分离 |




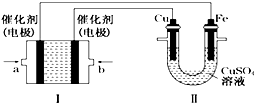 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题: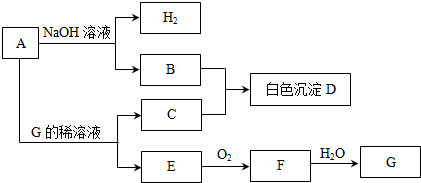

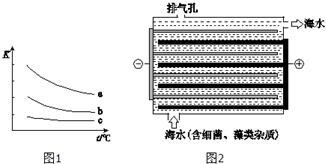 海水是巨大的化学资源宝库.
海水是巨大的化学资源宝库.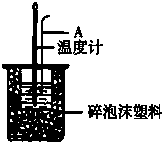 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.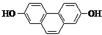 的有机物,在核磁共振氢谱上吸收峰的面积之比为
的有机物,在核磁共振氢谱上吸收峰的面积之比为