题目内容
19.阅读下面短文.光的散射与丁达尔效应
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射.在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应.产生丁达尔效应的实质是光的散射.
表1 分散系对可见光的不同作用
| 溶液 | 胶体 | 浊液 | |
| 光路示意图 |  |  | 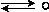 |
| 对光的主要作用 | 透射 | 散射 | 反射或折射 |
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象.
回答下列问题:
(1)产生丁达尔效应的实质是光的散射.
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的FeCl3溶液,继续煮沸至液体呈红褐色即可.
(3)胶体区别于其他分散系的本质特征是d(填序号).
a.胶体有丁达尔效应 b.胶体粒子可以透过滤纸
c.胶体的胶粒带有电荷 d.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是分散质的离子很小,对可见光的散射作用很微弱.
分析 (1)产生丁达尔效应的实质是光的散射;
(2)向沸水中滴入5~6滴饱和的FeCl3溶液,继续煮沸至液体呈红褐色可制得氢氧化铁胶体;
(3)胶体区别于其他分散系的本质特征是分散质微粒直径的大小不同;
(4)溶液分散质分子或离子更小,对可见光的散射作用很微弱.
解答 解:(1)在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应.产生丁达尔效应的实质是光的散射,故答案为:光的散射;
(2)向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变成红褐色,即可制得氢氧化铁胶体,故答案为:FeCl3;
(3)胶体区别于其他分散系的本质特征是分散质微粒直径的大小不同,胶体的分散质微粒直径介于1-100nm之间,故答案为:d;
(4)溶液分散质分子或离子更小,对可见光的散射作用很微弱,故答案为:分散质的离子很小,对可见光的散射作用很微弱.
点评 本题考查胶体的制备与性质,题目难度不大,注意根据题目信息解题,从题目中获取答案.

练习册系列答案
相关题目
9.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 生吃新鲜蔬菜要比熟吃时维生素C的损失大 | |
| B. | 水体中植物营养物质过多积累会引起水体富营养化 | |
| C. | 加强化石燃料的开采利用,能从根本上解决能源危机 | |
| D. | 推广使用煤液化技术,可减少二氧化碳等温室气体的排放 |
10.下列说法中,不正确的是( )
| A. |  钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀 | |
| B. |  钢铁表面水膜的酸性较强,发生析氢腐蚀 | |
| C. |  将锌板换成铜板对钢闸门保护效果更好 | |
| D. |  钢闸门作为阴极而受到保护 |
7.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 2 g H2所含原子数目为NA | |
| B. | 64 g SO2中含有的原子数为3 NA | |
| C. | 常温常压下,11.2 L Cl2含有的分子数为0.5 NA | |
| D. | 1 mol/L NaOH溶液中Na+的数目为NA |
14.某同学用如图所示的装置及药品进行酸性强弱比较的实验,下列说法不正确的是( )
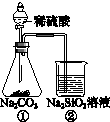

| A. | ①和②中发生的反应均为复分解反应 | |
| B. | 向Na2SiO3饱和溶液中滴酚酞溶液无明显现象 | |
| C. | 一段时间后②中有胶冻状物质生成 | |
| D. | 该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸 |
4.随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
| A. | 无水硫酸铜、蔗糖 | B. | 食盐、硫酸亚铁 | C. | 生石灰、硫酸亚铁 | D. | 硅胶、食盐 |
11.下列各组物质中,因反应物用量不同而发生不同化学反应的是( )
| A. | Cu与硝酸 | B. | SO2与NaOH溶液 | C. | Na与O2 | D. | Fe与Cl2 |
8.下列说法中正确的是( )
| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 二氧化碳的水溶液能够导电,故二氧化碳属于电解质 | |
| C. | 碳酸氢钠在水中电离的离子方程式为NaHCO3═Na++H++CO32- | |
| D. | 碳酸钠属于电解质 |