题目内容
15.如图是元素周期表的一部分,其中已标出了①-⑨九种元素.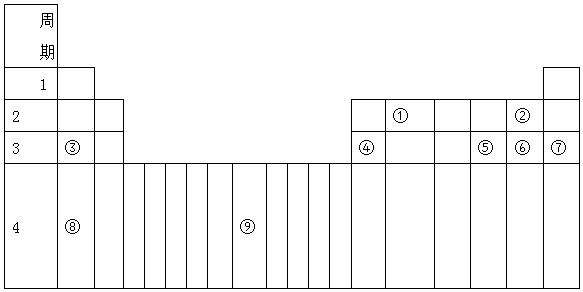
请用这九种元素回答下列问题:
(1)属于过渡元素的是⑨(用表中数字表示).
(2)非金属性最强的元素是K(填元素符号).
(3)元素⑤形成的两种氧化物中,能使品红溶液褪色的是SO2(填化学式).
(4)元素④的原子最外层电子数为3;
(5)写出元素③和元素⑥形成的化合物的化学式NaCl.
分析 由元素在周期表的位置可知,①-⑨九种元素分别为C、F、Na、Al、S、Cl、Ar、K、Fe,
(1)⑦为0族元素,⑨为ⅤⅢ族元素,其它为主族元素;
(2)同周期从左向右金属性减弱,同主族从上到下金属性增强;
(3)二氧化硫具有漂白性;
(4)Al位于ⅢA族;
(5)元素③和元素⑥形成的化合物为氯化钠.
解答 解:由元素在周期表的位置可知,①-⑨九种元素分别为C、F、Na、Al、S、Cl、Ar、K、Fe,
(1)副族、ⅤⅢ族元素统称为过渡元素,属于过渡元素的是⑨,故答案为:⑨;
(2)同周期从左向右金属性减弱,同主族从上到下金属性增强,则金属性最强的为K,故答案为:K;
(3)二氧化硫具有漂白性,能使品红溶液褪色的是SO2,故答案为:SO2;
(4)Al位于ⅢA族,族序数等于最外层电子数,则元素④的原子最外层电子数为3,故答案为:3;
(5)元素③和元素⑥形成的化合物为氯化钠,其化学式为NaCl,故答案为:NaCl.
点评 本题考查位置、结构与性质,为高频考点,把握元素在周期表的位置、元素及化合物性质为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
5.下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:则下列说法正确的是( )
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H1 | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g)△H2 | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O (g)?CO2(g)+H2(g)△H3 | K3 | ? | ? |
| A. | △H1<0,△H2>0 | |
| B. | 反应①②③的反应热满足关系:△H2-△H1=△H3 | |
| C. | 反应①②③的平衡常数满足关系:K1•K2=K3 | |
| D. | 要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施 |
6.下表为各物质中所含有的少量杂质以及除去这些杂质所选用的试剂或操作方法.下列表述正确的是( )
| 序号 | A | B | C | D |
| 物质 | KNO3溶液 | CO2 | 水 | 乙醇 |
| 杂质 | KOH | H2O(g) | 溴 | 水 |
| 除杂试剂 | FeCl3溶液 | - | 乙醇 | 生石灰 |
| 除杂 装置 | 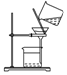 | 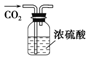 | 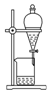 | 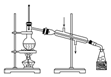 |
| A. | A | B. | B | C. | C | D. | D |
10.下列说法中,正确的是( )
| A. | 苯和甲苯可用酸性KMnO4溶液来鉴别 | |
| B. | 1mol苯或甲苯都可与3molH2发生加成反应 | |
| C. | 苯和甲苯中的所有原子都在同一平面上 | |
| D. | 苯乙烯、邻二甲苯、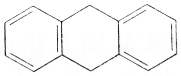 都是苯的同系物 都是苯的同系物 |
20.14g铜、银合金与一定量某浓度的硝酸溶液反应,金属完全溶解,放出的气体与1.12L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中银的质量是( )
| A. | 2.7g | B. | 5.4g | C. | 8.1g | D. | 10.8g |
7.下列有关气体摩尔体积的描述中正确的是( )
| A. | 相同物质的量的气体摩尔体积一定相同 | |
| B. | 通常状况下的气体摩尔体积约为22.4L | |
| C. | 标准状况下的气体摩尔体积约为22.4L | |
| D. | 单位物质的量的气体所占的体积就是气体摩尔体积 |
4.下列有关热化学方程式书写及对应表述均正确的是( )
| A. | 稀醋酸与0.1 mol•L-1NaOH反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1 | |
| B. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热充分反应,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热△H=-110.5 kJ•mol-1 |
14.NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 60克SiO2含有2NA个Si-O共价键 | |
| B. | 实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA | |
| C. | 1L 0.2mol•L-1Al2(SO4)3溶液中的离子总数为NA | |
| D. | 标准状况下,22.4mLH2O约含有 3.73NA个原子 |