题目内容
(1)新切开的金属钠,切面呈 色,在空气中很快变暗,有关的化学方程式是 .
(2)将小块金属钠投入盛有水的烧杯里,钠熔化成闪亮的小球,说明 .
(3)因此,钠通常保存在 中,钠元素在自然界存在的形态为 .
(4)过氧化钠可用作于供氧剂,写出过氧化钠与二氧化碳反应的化学方程式 .
(2)将小块金属钠投入盛有水的烧杯里,钠熔化成闪亮的小球,说明
(3)因此,钠通常保存在
(4)过氧化钠可用作于供氧剂,写出过氧化钠与二氧化碳反应的化学方程式
考点:钠的化学性质
专题:
分析:(1)根据金属钠的物理性质以及在常温下能与氧气发生反应;
(2)根据金属钠的物理性质、金属钠能与水反应得到碱和氢气,该反应放热;
(3)根据金属钠的密度以及化学性质来判断;
(4)过氧化钠可以和二氧化碳反应生成碳酸钠和氧气.
(2)根据金属钠的物理性质、金属钠能与水反应得到碱和氢气,该反应放热;
(3)根据金属钠的密度以及化学性质来判断;
(4)过氧化钠可以和二氧化碳反应生成碳酸钠和氧气.
解答:
解:(1)金属钠为银白色,新切开的金属钠空气中很快变暗,是因为氧气发生了化学反应生成了氧化钠,故答案为:银白;4Na+O2=2Na2O;
(2)金属钠的熔点低,金属钠能与水反应该反应为放热反应,所以金属钠熔化成闪亮的小球,故答案为:金属钠的熔点低,该反应为放热反应;
(3)金属钠空气中很快变暗又能与水迅速反应,又钠的密度比煤油小,故答案为:煤油;化合态;
(4)过氧化钠与二氧化碳反应生成碳酸钠和氧气,即2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2.
(2)金属钠的熔点低,金属钠能与水反应该反应为放热反应,所以金属钠熔化成闪亮的小球,故答案为:金属钠的熔点低,该反应为放热反应;
(3)金属钠空气中很快变暗又能与水迅速反应,又钠的密度比煤油小,故答案为:煤油;化合态;
(4)过氧化钠与二氧化碳反应生成碳酸钠和氧气,即2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2.
点评:此题是对钠的性质及其过氧化钠的性质考查,解题的重点是对钠与水反应的有关问题,特别是物质的性质的反应的掌握,属基础性知识考查题.

练习册系列答案
相关题目
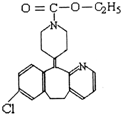 开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )
开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )| A、该有机物的分子式是C22H23N2O2Cl |
| B、分子中含有四个六元环,其中有一个是苯环 |
| C、1mol分子发生水解反应后能得到2mol新分子 |
| D、1mol分子发生加成反应需要8mol H2 |
下列离子方程式书写正确的是 ( )
| A、过量二氧化硫气通入到漂白粉溶液中Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| B、Ba(OH)2溶液中滴入几滴硫酸铜溶液:Cu2++2OH-═Cu(OH)2↓ |
| C、用湿润的醋酸铅试纸检验硫化氢:Pb2++H2S═PbS↓+2H+ |
| D、碳酸镁溶液中加入过量的澄清石灰水:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O |
下列各化学式中,只表示一种纯净物的是( )
| A、C2H4O2 |
| B、C3H6 |
| C、C2H3Br |
| D、C3H6O |
下列关于有机化合物的说法正确的是( )
| A、甲烷和乙烯都可以与氯气反应 |
| B、异丁烷与2-甲基丁烷互为同分异构体 |
| C、油脂和淀粉都是高分子化合物 |
| D、乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
2011年为国际化学年,主题为“化学-我们的生活,我们的未来”.下列说法不正确的是( )
| A、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、工业上冶炼Al,使用Al2O3而不使用AlCl3,是因为AlCl3是共价化合物,熔融不导电 |
| D、二氧化硫可用于漂白纸浆、毛、丝等,还可用于杀菌消毒 |
下列无色溶液中,能大量共存的离子组是( )
| A、Ba2+、Ca2+、C1-、NO3- |
| B、Ca2+、A13+、Fe3+、CO32- |
| C、NH4+、K+、HSO3-、ClO- |
| D、Na+、K+、MnO4-、I- |
下列物质中,只有在溶液中才能导电的电解质是( )
| A、NaCl |
| B、酒精 |
| C、H2SO4 |
| D、SO3 |
下列物质的水溶液中,其电离方程式正确的是( )
| A、H2SO4=H2++SO42- |
| B、NaHSO4=Na++HSO4- |
| C、Na2CO3=2Na++CO32- |
| D、Ca(OH)2=Ca2++OH- |