题目内容
13.下列说法不正确的是( )| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(M+)>c(H+)>c(OH-)>c(A-) | |
| B. | 中和相同体积、相同物质的量浓度的①硫酸,②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3 | |
| C. | 稀氨水中部分粒子的浓度大小关系:c(NH3•H2O)>c(OH-)>c(NH4+)>c(H+) | |
| D. | 1mol/LNaX和1mol/LNaY两种盐溶液中c(X-)=c(Y-)+c(HY),则HX为强酸 |
分析 A.不知道酸碱的体积,无法判断混合溶液的酸碱性;
B.根据酸中氢离子判断;
C.氨水部分电离,水也能电离;
D.根据物料守恒判断.
解答 解:A.pH=2的HA溶液与pH=12的MOH溶液任意比混合,不知道二者的体积大小,无法判断混合溶液中酸碱性,故A错误;
B.中和相同体积、相同物质的量浓度的①硫酸,②盐酸和③醋酸,由于盐酸和醋酸为一元酸,硫酸为二元酸,所以所需相同浓度的NaOH溶液的体积关系:V1>V2=V3,故B正确;
C.氨水部分电离,所以c(NH3•H2O)>c(OH-),水也能电离,所以溶液中c(OH-)>c(NH4+),则稀氨水中部分粒子的浓度大小关系:c(NH3•H2O)>c(OH-)>c(NH4+)>c(H+),故C正确;
D.1mol/LNaX和1mol/LNaY两种盐溶液中c(X-)=c(Y-)+c(HY),根据物料守恒可知,X-没发生水解,即HX为强酸,故D正确.
故选A.
点评 本题考查了混合溶液酸碱性的判断、盐的水解和弱电解质的电离,题目难度中等,侧重于考查学生对基础知识的应用能力,注意电荷守恒和物料守恒的应用.

练习册系列答案
相关题目
3.下列离子方程式正确的是( )
| A. | 盐酸与氨水的反应:H++OH-═H2O | |
| B. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 氯气通入FeCl3溶液中:Cl2+Fe2+═Fe3++2Cl- |
4.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则氢气的燃烧热为-241.8 kJ•mol-1 | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量 | |
| C. | 己知2C(s)+2O2(g)═2CO2(g)△H=a;2C(s)+O2(g)=2CO(g);△H=b,则a>b | |
| D. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
1.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,它们物质的量必相等 | |
| B. | 在任何情况下,等质量的氮气和一氧化碳所含分子数必相等 | |
| C. | 1L一氧化碳气体的质量一定比1L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中,所含的H+数目一定相等 |
8.下列物质与FeCl3溶液不能发生化学变化的是( )
①AgNO3溶液
②Na2SO4溶液
③CuO
④SO2
⑤稀硝酸
⑥H2O2.
①AgNO3溶液
②Na2SO4溶液
③CuO
④SO2
⑤稀硝酸
⑥H2O2.
| A. | ②④⑤ | B. | ①③⑥ | C. | ②③ | D. | ②⑤ |
18.储存浓H2SO4的铁罐外口常会出现严重的腐蚀现象,这体现了( )
| A. | 浓H2SO4的吸水性和酸性 | |
| B. | 浓H2SO4的脱水性和吸水性 | |
| C. | 浓H2SO4的强氧化性和吸水性 | |
| D. | 浓H2SO4的吸水性和稀H2SO4的通性(酸性) |
5.下列有关实验现象的描述正确的是( )
| A. | 铁丝在空气中被点燃,火星四射 | |
| B. | 氧化铁放入氢氧化钠溶液中,生成红褐色沉淀 | |
| C. | 点燃氢气和一氧化碳的混合气体,发生猛烈爆炸 | |
| D. | 氯化铜溶液中滴入氢氧化钠溶液,产生蓝色沉淀 |
2.在通风橱中进行的下列实验:
下列说法中不正确的是( )
| 步骤 | 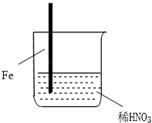 | 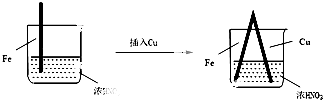 | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
3.关于现行的元素周期表的说法正确的是( )
| A. | 元素周期表有8个副族 | B. | 元素周期表有7个周期 | ||
| C. | 短周期是指第一、二周期 | D. | IA族的元素全部是金属元素 |