题目内容
13.电子工业常用30%FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.(1)检验溶液中存在Fe3+所用试剂是KSCN溶液,观察到的现象是溶液变成红色.
(2)写出FeCl3溶液与铜发生反应的离子方程式:2Fe3++Cu=Cu2++2Fe2+;
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤
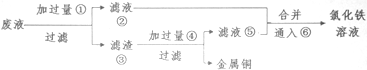
A.请写出上述实验中有关物质的化学式:①Fe、⑤FeCl2;
B.写出相关反应的离子方程式Fe+Cu2+═Cu+Fe2+、Fe+2H+=Fe2++H2↑、2Fe2++Cl2=2Fe3++2Cl-.
分析 (1)检验溶液中Fe3+存在通常用KSCN溶液,溶液变红说明Fe3+存在;
(2)用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2;
(3)腐蚀废液中含有氯化铜、氯化亚铁,加入过量的铁可以和氯化铜反应生成金属铜和氯化亚铁,故①为Fe,经过滤所得滤液是氯化亚铁,滤渣是金属铜和过量的铁,铜不能盐酸反应,而金属铁可以,加入过量盐酸可以将铜分离,得到的滤液为氯化亚铁,滤液合并后通入氯气,能将亚铁离子氧化为三价铁,以此解答该题.
解答 解:(1)检验溶液中Fe3+存在的试剂是KSCN溶液,发生Fe3++3SCN-=Fe(SCN)3,则证明Fe3+存在的现象是溶液变成红色,故答案为:KSCN溶液;溶液变成红色;
(2)铜与氯化铁反应生成氯化铁、氯化亚铁,反应离子方程式为:2Fe3++Cu=Cu2++2Fe2+,
故答案为:2Fe3++Cu=Cu2++2Fe2+;
(3)①腐蚀废液中含有氯化铜、氯化亚铁即氯化铁,加入过量的铁可以和氯化铁反应生成氯化亚铁,和氯化铜反应生成金属铜和氯化亚铁,故滤液②是氯化亚铁,滤渣③是金属铜和过量的铁,铜不能盐酸反应,而金属铁可以,加入足量的盐酸可以将铜分离,得到的滤液⑤是氯化亚铁,氯气具有氧化性,能将亚铁离子氧化为三价铁,故⑥是氯气,
故答案为:Fe;FeCl2;
②反应①为Fe+Cu2+═Cu+Fe2+,反应④为Fe+2H+=Fe2++H2↑,反应⑥为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:Fe+Cu2+═Cu+Fe2+、Fe+2H+=Fe2++H2↑、2Fe2++Cl2=2Fe3++2Cl-.
点评 本题考查化学工艺流程、原电池等,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,把握发生的反应及现象、离子检验方法为解答的关键,难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | Mg2+、Cl-、OH- | B. | Na+、CO32-、OH- | C. | Fe2+、H+、CO32- | D. | Fe3+、K+、OH- |
| A. | CH2=CH3 | B. | CH2=CH-CH2OH | C. | CH3=CH-COOH | D. | CH2=CH-COOCH3 |
| A. | 稀盐酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O | |
| C. | 石灰石上滴加稀盐酸:CaCO3+2H+═Ca2++H2CO3 | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| A. | NaCl | B. | H2S | C. | SO2 | D. | HNO3 |
| A. | Cl-的结构示意图: | |
| B. | 乙酸的结构示意图:C2H4O2 | |
| C. | 硫酸的电离方程式:H2SO4═H2++SO42- | |
| D. | 氯化钠的电子式: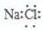 |
| A. | 用电解法精炼铜时,粗铜作阴极、精铜作阳极 | |
| B. | 在镀件上电镀铜时,用金属铜作阳极 | |
| C. | 在电解池中,铜作电极时,溶液中的阴离子在铜极上失电子 | |
| D. | 电解饱和食盐水制稀硫酸制Cl2、H2时,可用金属铜作阳极 |
(1)已知某温度下某反应的化学平衡常数表达式为:K=$\frac{c({H}_{2}O)}{c(CO)•c({H}_{2})}$,所对应的化学反应方程式为:CO(g)+H2(g)?C(s)+H2O(g).
(2)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b)kJ/mol(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:
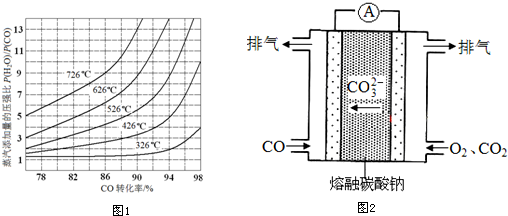
对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(C{O}_{2})P({H}_{2})}{P(CO)P({H}_{2}O)}$,提高p[H2O(g)]:p(CO)比,则Kp不变(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]:p(CO)=3~5.其原因可能是①该温度下催化剂活性最大②该压强比下,反应物转化率已经接近98%.
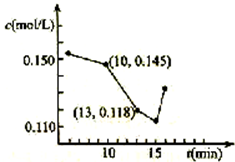
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:CO-2e-+CO32-=2CO2.
 对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下:
对低品位的菱镁矿(主要成份是MgCO3和CaCO3)的综合利用意义重大.矿石经煅烧、消化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离.碳化反应的化学方程式如下: