题目内容
2.下列说法中,正确的是( )| A. | 干冰升华时要吸收热量,所以这是吸热反应 | |
| B. | 化学反应中能量的变化都表现为热量的变化 | |
| C. | 1 mol Ba(OH)2与1 mol H2SO4反应释放的热量为Q,则Q为它们反 应的中和热 | |
| D. | 物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能 释放出来 |
分析 A.干冰升华属于物理变化;
B.化学反应中能量的变化主要表现为热量的变化;
C.中和热规定生成1mol液态水;
D.物质燃烧是放热反应,是将化学能转化为热能.
解答 解:A.干冰升华属于物理变化,因此不是吸热反应,故A错误;B.化学反应中能量的变化主要表现为热量的变化,还有光能、电能等形式的变化,故B错误;
C.1 mol Ba(OH)2与1 mol H2SO4反应生成2mol水,而且还有硫酸钡生成,因此中和热不是Q,故C错误;
D.物质燃烧是放热反应,是将“储存”在物质内部的化学能转化为热能释放出来,故D正确;
故选D.
点评 本题主要考查了化学反应中能量变化,题目难度不大,注意物理变化过程中吸热或放热不能称为吸热反应和放热反应.

练习册系列答案
相关题目
12. 太阳能的开发和利用是21世纪的一个重要课题.
太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
其中最适宜作储能介质的是B(填字母).
A、CaCl2•6H2O B、Na2SO4•10H2O C、Na2HPO4•12H2O D、Na2S2O3•5H2O
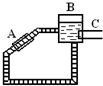
②如图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据
对水的密度的认识,你估计在阳光照射下水将沿顺(填“顺”或“逆”)时针方向流动.
 太阳能的开发和利用是21世纪的一个重要课题.
太阳能的开发和利用是21世纪的一个重要课题.①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热/KJ•mol-1 | 参考价格/元•kg-1 |
| CaCl2•6H2O | 29.0 | 37.3 | 780~850 |
| Na2SO4•10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4•12H2O | 36.1 | 100.1 | 1600~2000 |
| Na2S2O3•5H2O | 48.5 | 49.7 | 1400~1800 |
A、CaCl2•6H2O B、Na2SO4•10H2O C、Na2HPO4•12H2O D、Na2S2O3•5H2O
②如图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据
对水的密度的认识,你估计在阳光照射下水将沿顺(填“顺”或“逆”)时针方向流动.
13.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X 不同周期.下列说法一定正确的是( )
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | X、Y、Z不能形成共价化合物 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
17.下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
| A. | 硫化氢在氧气中燃烧 | B. | 铁在硫蒸气中燃烧 | ||
| C. | 二氧化硫通入石灰水 | D. | 锌粉和硫酸反应 |
7.下列哪些能源属于二次能源( )
| A. | 风力 | B. | 电力 | C. | 原煤 | D. | 流水 |
14.用下列装置完成相关实验,不合理的是( )
| A. |  用a趁热过滤提纯苯甲酸 | B. |  用b制备并检验乙烯 | ||
| C. | 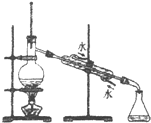 用c制无水乙醇 | D. |  用d分离硝基苯与水 |

 .
.
 .
.