题目内容
下列表述中正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则1mol氢气燃烧放出热量为483.6 kJ |
| B、由C(石墨,s)═C(金刚石,s)△H=+11.9 kJ?mol-1可知,石墨比金刚石稳定 |
| C、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
| D、化学变化不一定都伴随着能量的变化 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A.由2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则1mol氢气燃烧放出热量为241.8 kJ;
B.能量越低的物质就越稳定;
C.反应热取决于反应物总能量和生成物总能量的大小关系;
D.化学变化一定都伴随着能量的变化.
B.能量越低的物质就越稳定;
C.反应热取决于反应物总能量和生成物总能量的大小关系;
D.化学变化一定都伴随着能量的变化.
解答:
解:A.由2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则1mol氢气燃烧放出热量为241.8 kJ,故A错误;
B.依据热化学方程式可知石墨变化为金刚石是吸热反应,金刚石能量高于石墨,说明金刚石不如石墨稳定,故B正确;
C.反应热取决于反应物总能量和生成物总能量的大小关系,与反应的条件无关,△H相同,故C错误;
D.化学变化一定都伴随着能量的变化,故D错误.
故选B.
B.依据热化学方程式可知石墨变化为金刚石是吸热反应,金刚石能量高于石墨,说明金刚石不如石墨稳定,故B正确;
C.反应热取决于反应物总能量和生成物总能量的大小关系,与反应的条件无关,△H相同,故C错误;
D.化学变化一定都伴随着能量的变化,故D错误.
故选B.
点评:本题考查较为综合,涉及化学反应与能量的变化等问题,侧重于化学知识的综合应用,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤,不正确的操作顺序是( )
| A、⑤③②①⑤④ |
| B、⑤③①②⑤④ |
| C、⑤②③①⑤④ |
| D、⑤②①③⑤④ |
下列有关反应热的叙述正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| B、C(石墨,s)═C(金刚石,s)△H>0,所以金刚石比石墨稳定 |
| C、已知碳的燃烧热为ykJ/mol,当7.2g的碳在12.8g的氧气中燃烧,至反应物耗尽并放出xkJ的热量,则可求出1mol碳与氧气反应生成1mol一氧化碳气体时△H=-(2.5x-0.5y)kJ/mol |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
下列反应中属于氧化还原反应的是( )
| A、2NaHCO3=Na2CO3+CO2↑+H2O |
| B、2KMnO4=K2MnO4+MnO2+O2↑ |
| C、Ca(OH)2+CO2=CaCO3↓+H2O |
| D、Cu(OH)2+H2SO4=CuSO4+2H2O |
下列溶液中c(Cl-)与50mL 1mol/L AlCl3溶液中c(Cl-)相等是( )
| A、100mL 3mol/L KCl溶液 |
| B、25mL 2mol/L AlCl3溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、25mL 1.5mol/L MgCl2溶液 |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是( )
A、甲烷与氯气反应制氯仿:CH4+3Cl2
| ||
B、烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2
| ||
C、甲烷、CO合成乙酸乙酯:2CH4+2CO
| ||
D、乙烯合成聚乙烯nCH4+2CO
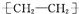 |
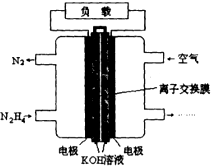 肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.
肼(N2H4)是火箭发射常用的燃料.一种以肼(N2H4)为燃料的电池装置如图所示. 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质.