题目内容
13.为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论正确的是( )| A. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,可看到有氢气生成 | |
| B. | 将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度NaOH溶液反应,前者速率大于后者 | |
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 | |
| D. | 大理石和盐酸反应制取CO2,增加大理石的用量可加快反应速率 |
分析 A.铜不能置换出氢气;
B.镁与氢氧化钠溶液不反应;
C.催化剂能加快反应速率;
D.增大固体的用量化学反应速率不变.
解答 解:A.铜为不活泼金属,与稀硫酸不反应,故A错误;
B.镁与氢氧化钠溶液不反应,不能用于比较反应速率,故B错误;
C.催化剂能加快反应速率,在氯酸钾分解的试验中,二氧化锰起到催化剂的作用,故C正确;
D.增大固体的用量,浓度不变,则化学反应速率不变,故D错误.
故选C.
点评 本题考查外界条件对化学反应速率的影响,题目难度不大,注意B项,为易错点,物质的性质是影响化学反应速率的主要因素.

练习册系列答案
相关题目
3.下列各组离子,在水溶液中能大量共存的是( )
(1)I-、ClO-、NO3-、H+
(2)k+、Ag(NH3)2+、NO3-、H+
(3)NH4+、SO42-、Cl-、HCO3-
(4)Fe3+、Cu2+、SO42-、Cl-
(5)H+、k+、AlO2-、C6H15O-
(6)Pb2+、Na+、SO42-、NO3-.
(1)I-、ClO-、NO3-、H+
(2)k+、Ag(NH3)2+、NO3-、H+
(3)NH4+、SO42-、Cl-、HCO3-
(4)Fe3+、Cu2+、SO42-、Cl-
(5)H+、k+、AlO2-、C6H15O-
(6)Pb2+、Na+、SO42-、NO3-.
| A. | (1)和(6) | B. | (3)和(4) | C. | (2)和(4) | D. | (2)和(5) |
1.下列是除去括号内杂质的有关操作,其中正确的是( )
| A. | 乙醇(乙酸)--加水,振荡静置后分液 | |
| B. | SO2(CO2)--氢氧化钠溶液 | |
| C. | 乙烯(乙炔)--将气体通过盛KMnO4溶液的洗气瓶 | |
| D. | 苯(苯酚)--加足量NaOH溶液,振荡静置后分液 |
18.质量比为2:1的H2SO4和H3PO4,它们所含氢原子物质的量之比是( )
| A. | 2:1 | B. | 2:3 | C. | 4:3 | D. | 1:1 |
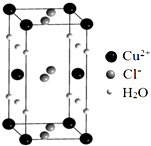 将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出晶体Cu(NH3)4SO4•H2O•SO42-
将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出晶体Cu(NH3)4SO4•H2O•SO42-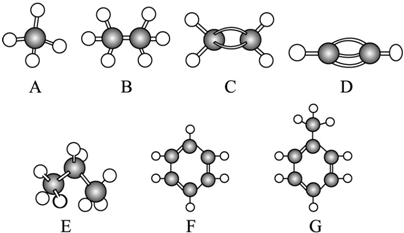

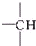 和
和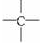 等结构组成的.如果某烷烃分子中同时存在这4种基团,所含碳原子数又最少,这种烃分子应含8个碳原子.
等结构组成的.如果某烷烃分子中同时存在这4种基团,所含碳原子数又最少,这种烃分子应含8个碳原子.