题目内容
6.在一密闭容器中进行反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ/mol测得CH4的物质的量浓度随反应时间的变化如图1所示.0-5min内用H2表示反应速率为0.3mol•L-1•min-1;反应中处于平衡状态的时间段为;10min时,改变的外界条件可能是:升高温度.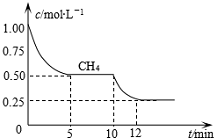
分析 0-5min时甲烷平均反应速率=$\frac{1-0.50}{5-0}$mol/(L.min)=0.1mol/(L.min),再根据同一化学反应中同一时间段内各物质的反应速率之比等于其计量数之比计算氢气反应速率,10min改变条件时甲烷的物质的量浓度不变,但随着时间的延长,甲烷浓度降低,说明不是通过改变压强或甲烷浓度而发生的平衡移动,且平衡正向移动,10-12min时甲烷的平均反应速率=$\frac{0.50-0.25}{12-10}$mol/(L.min)=0.125mol/(L.min)>0.1mol/(L.min),改变的条件是温度,据此分析解答.
解答 解:0-5min时甲烷平均反应速率=$\frac{1-0.50}{5-0}$mol/(L.min)=0.1mol/(L.min),同一化学反应中同一时间段内各物质的反应速率之比等于其计量数之比,则氢气的平均反应速率=3v(CH4)=0.3mol/(L.min),10min改变条件时甲烷的物质的量浓度不变,但随着时间的延长,甲烷浓度降低,说明不是通过改变压强或甲烷浓度而发生的平衡移动,且平衡正向移动,10-12min时甲烷的平均反应速率=$\frac{0.50-0.25}{12-10}$mol/(L.min)=0.125mol/(L.min)>0.1mol/(L.min),改变的条件是温度,该反应的正反应是吸热反应,所以改变的条件是升高温度,
故答案为:0.3;升高温度.
点评 本题考查图象分析计算有关计算,为高频考点,侧重考查学生分析判断及计算能力,明确外界条件对化学反应速率、化学平衡移动影响原理是解本题关键,知道化学反应速率与计量数之间的关系,题目难度不大.

练习册系列答案
相关题目
17.“春蚕到死丝方尽,蜡炬成灰泪始干.”中的“丝”和“泪”分别是指( )
| A. | 油脂,纤维素 | B. | 蛋白质,烃 | C. | 纤维素,烃 | D. | 蛋白质,油脂 |
14.下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的( )
| A. | 6和8 | B. | 19和16 | C. | 12和17 | D. | 7和8 |
1.常温下,现有电解质溶液:①NaClO ②NaOH ③NaHCO3 ④CH3COONa,当几种溶液的pH相同时,其物质的量浓度由大到小的顺序排列正确的是( )
| A. | ②①③④ | B. | ①③④② | C. | ④③①② | D. | ③④②① |
11.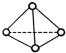 科学家己获得了极具理论研究意义的N4分子,其结构为正四面体型(如图所示),分子中每个氮原子最外电子层都满足8电子结构.己知断裂1mol N-N键吸收192kJ热量,断梨1mol N-N键吸收946kJ热量,则下列叙述中正确的是( )
科学家己获得了极具理论研究意义的N4分子,其结构为正四面体型(如图所示),分子中每个氮原子最外电子层都满足8电子结构.己知断裂1mol N-N键吸收192kJ热量,断梨1mol N-N键吸收946kJ热量,则下列叙述中正确的是( )
 科学家己获得了极具理论研究意义的N4分子,其结构为正四面体型(如图所示),分子中每个氮原子最外电子层都满足8电子结构.己知断裂1mol N-N键吸收192kJ热量,断梨1mol N-N键吸收946kJ热量,则下列叙述中正确的是( )
科学家己获得了极具理论研究意义的N4分子,其结构为正四面体型(如图所示),分子中每个氮原子最外电子层都满足8电子结构.己知断裂1mol N-N键吸收192kJ热量,断梨1mol N-N键吸收946kJ热量,则下列叙述中正确的是( )| A. | 1molN4气体转化为N2时要吸收206 kJ能量 | |
| B. | N4是一种比N2更稳定的分子 | |
| C. | 1molN4气体转化为N2时要放出740 kJ能量 | |
| D. | N4是N2的同位素 |
16.下列物质对应的电子式书写正确的是( )
| A. | NH4Br: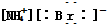 | B. | CaCl2: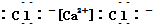 | ||
| C. | Na2O2: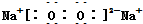 | D. | N2:N??N |
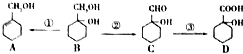 已知有机物A、B、C、D在一定条件下有如图所示的转化关系:
已知有机物A、B、C、D在一定条件下有如图所示的转化关系: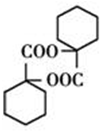 、
、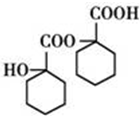 .
. .
.