题目内容
某气体对氧气的相对密度为2,则该气体可能为( )
| A、H2 |
| B、O2 |
| C、CO2 |
| D、SO2 |
考点:物质的量的相关计算
专题:计算题
分析:根据相对氢气的密度计算混合气体的平均摩尔质量,然后根据选项确定结果.
解答:
解:气体对氧气的相对密度为2,则混合气体的平均摩尔质量为32g/mol×2=64g/mol,即该气体的相对分子量为64,所以是二氧化硫气体,故选D.
点评:本题考查相对分子质量的计算,难度不大,相对分子质量的常用计算方法有:利用原子的相对原子质量计算,比较容易.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式书写正确的是( )
| A、醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O |
| B、过量的氨水滴加到氯化铝溶液中:Al3++4OH-═AlO2-+2H2O |
| C、次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
| D、Na2O2溶于水产生O2:2Na2O2+2H2O═4Na++4OH-+O2↑ |
 如图装置中具支试管内盛有pH=4的雨水和生铁片,小试管内为红墨水.观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面.以下有关解释合理的是( )
如图装置中具支试管内盛有pH=4的雨水和生铁片,小试管内为红墨水.观察:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面.以下有关解释合理的是( )| A、生铁片中的碳是原电池的阳极 |
| B、导管内液面下降时,碳极反应式为:O2+2H2O+4e-→4OH- |
| C、具支试管中溶液pH逐渐减小 |
| D、生铁片既发生析氢腐蚀,又发生了吸氧腐蚀 |
下列关于物质分类的说法正确的是( )
| A、根据酸分子中含有的氢原子个数、将酸分为一元酸、二元酸和多元酸 |
| B、混合物:铝热剂、福尔马林、水玻璃、漂白粉 |
| C、根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 |
| D、明矾、水银、烧碱、硫酸均为强电解质 |
根据下列化学实验事实得出的结论一定正确的是( )
| A、向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解.结论:该溶液中含有SO42- |
| B、向某无色溶液中加入足量盐酸,产生能使澄清石灰水变浑浊的气体.结论:该溶液中含有CO32-或HCO3- |
| C、向1 mL浓度均为0.05 mol/L的NaCl、NaI混合溶液中滴加2滴0.01 mol/L的AgNO3溶液,振荡,沉淀呈黄色.结论:Ksp(AgCl)<Ksp(AgI) |
| D、向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝.结论:该溶液中有NH4+ |
 甲醇、乙醇是重要的有机化工原料,有着重要的用途和应用前景.
甲醇、乙醇是重要的有机化工原料,有着重要的用途和应用前景.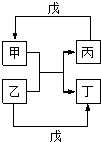 甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )