题目内容
2.下列离子方程式表达正确的是( )| A. | SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr | |
| B. | 向漂白粉稀溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
分析 A.溴化氢为强酸,应拆成离子形式;
B.二氧化碳过量,反应生成次氯酸和碳酸氢钙;
C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性则消耗的硫酸氢钠与氢氧化钡物质的量之比为2:1;
D.不符合反应客观事实,三价铁离子能够氧化碘离子.
解答 解:A.SO2通入溴水中,离子方程式:SO2+2H2O+Br2═4H++SO42-+2Br-,故A错误;
B.向漂白粉稀溶液中通入过量CO2,离子方程式:ClO-+CO2+H2O═HClO+HCO3-,故B正确;
C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液显中性,离子方程式:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.氢氧化铁溶于氢碘酸中的离子反应为2I-+2Fe(OH)3+6H+═2Fe2++6H2O+I2,故D错误;
故选:B.
点评 本题考查离子反应方程式书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,题目难度不大,注意化学式的拆分、注意反应遵循客观事实.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
12.下列关于氯气的叙述中,正确的是( )
| A. | 氯气以液态形式存在时可称为氯水或液氯 | |
| B. | 红热的铜丝在氯气中燃烧,冒蓝色烟 | |
| C. | 有氯气参加的化学反应必须在溶液中进行 | |
| D. | 钠在氯气中燃烧生成白色固体氯化钠 |
13.某气态烃1mol能与2molHCl加成,所得的加成产物每摩尔又能与8molCl2反应,最后得到一种只含C、Cl两种元素的化合物,则气态烃为( )
| A. | 丙烯 | B. | 1-丁炔 | ||
| C. | 丁烯 | D. | 2-甲基-1,3-丁二烯 |
10.目前世界上60%的镁是从海水中提取的.主要步骤如下: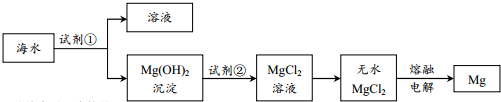
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 为使海水中的MgSO4转化成Mg(OH)2,试剂①可选择石灰乳 | |
| B. | 加入试剂①后,分离得到Mg(OH)2沉淀的方法是过滤 | |
| C. | 加入试剂②反应的离子方程式为:OH-+H+=H2O | |
| D. | 通过电解熔融的无水MgCl2得到48gMg,共转移4mol电子 |
17.下列说法正确的是( )
| A. | 蔗糖在硫酸催化下水解,只生成葡萄糖 | |
| B. | 石油的裂解、煤的干馏都是化学变化 | |
| C. | 1L1mol•L-1AlCl3溶液中含Al3+数目为6.02×1023 | |
| D. | 等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH 途径a:Al$→_{点燃}^{O_{2}}$Al2O3$\stackrel{NaOH溶液}{→}$NaAlO2;途径b:Al$\stackrel{NaOH溶液}{→}$NaAlO2 |
7.常温下,下列有关溶液的说法正确的是( )
| A. | 向0.10mol•L-1NaHSO3溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略):c(Na+)>c(SO32-)>c(NH4+) | |
| B. | 0.1mol/L醋酸钠溶液20mL与0.1mol•L-1盐酸10mL混合后的溶液中:c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| C. | 已知Kw(HF)>Kw(CH3COOH),pH相等的NaF与CH3COOK两溶液中:c(Na+)-c(F-)>c(K+)-c(CH3COO-) | |
| D. | 0.1mol•L-1醋酸溶液和0.2mol•L-1醋酸钠溶液等体积混合后的溶液中:3c(H+)+2c(CH3COOH)=c(CH3COO-)+3c(OH-) |
14.为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间.
(1)设计实验2和实验3的目的是研究H2O2的浓度对化学反应速率的影响.
(2)为研究温度对化学反应速率的影响,可以将实验2和实验4作对比(填序号).
(3)将实验1和实验2作对比,t1>t2(填“>”、“<”或“=”).
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•L-1 KI溶液 ②0.1mol•L-1 FeCl3溶液 ③0.1mol•L-1 FeCl2溶液 ④0.1mol•L-1 盐酸 ⑤0.1mol•L-1KSCN溶液 ⑥CCl4
实验步骤:(1)取5mL 0.1mol•L-1 KI溶液,再滴加几滴0.1mol•L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂⑤(填序号),现象溶液显血红色,说明此反应存在一定的限度.
Ⅲ.N2O4可分解为NO2.在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2).c(NO2)随时间变化的数据记录如图所示.

(1)反应容器中最后剩余的物质有N2O4和NO2,其中N2O4的物质的量为0.004mol.
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后不变.
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间.
| 序号 | 反应 温度/℃ | c(H2O2)/ mol•L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
(2)为研究温度对化学反应速率的影响,可以将实验2和实验4作对比(填序号).
(3)将实验1和实验2作对比,t1>t2(填“>”、“<”或“=”).
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•L-1 KI溶液 ②0.1mol•L-1 FeCl3溶液 ③0.1mol•L-1 FeCl2溶液 ④0.1mol•L-1 盐酸 ⑤0.1mol•L-1KSCN溶液 ⑥CCl4
实验步骤:(1)取5mL 0.1mol•L-1 KI溶液,再滴加几滴0.1mol•L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂⑤(填序号),现象溶液显血红色,说明此反应存在一定的限度.
Ⅲ.N2O4可分解为NO2.在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2).c(NO2)随时间变化的数据记录如图所示.

(1)反应容器中最后剩余的物质有N2O4和NO2,其中N2O4的物质的量为0.004mol.
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后不变.
11.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | CH4(C2H4) | Br2水 | 洗气 |
| B | C6H6(Br2) | Fe粉 | 蒸馏 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |