题目内容
从海水中提取部分物质的过程如图所示
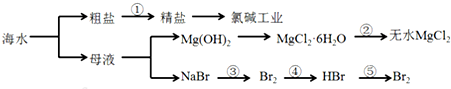
下列有关说法不正确的是( )

下列有关说法不正确的是( )
| A、从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能的过程 |
| B、过程②中结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| C、经过③④实现了溴元素的富集 |
| D、电解MgCl2溶液制取Mg单质 |
考点:海水资源及其综合利用
专题:元素及其化合物
分析:A、氯碱工业是电解饱和氯化钠溶液发生氧化还原反应,电能转化为化学能;
B、过程②是加热氯化镁晶体失去结晶水得到固体氯化镁,镁离子在水溶液中会水解分析;
C、步骤③④是生成溴单质被还原剂吸收生成溴离子,加入氧化剂重新生成溴单质的过程,是富集溴元素的过程;
D、电解熔融氯化镁制备金属镁.
B、过程②是加热氯化镁晶体失去结晶水得到固体氯化镁,镁离子在水溶液中会水解分析;
C、步骤③④是生成溴单质被还原剂吸收生成溴离子,加入氧化剂重新生成溴单质的过程,是富集溴元素的过程;
D、电解熔融氯化镁制备金属镁.
解答:
解:A、氯碱工业是电解饱和氯化钠溶液发生氧化还原反应,是电能转化为化学能的过程,故A正确;
B、过程②是加热氯化镁晶体失去结晶水得到固体氯化镁,镁离子在水溶液中会水解,结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2,故B正确;
C、步骤③④是生成溴单质被还原剂吸收生成溴离子,加入氧化剂重新生成溴单质的过程,是富集溴元素的过程,故C正确;
D、电解熔融氯化镁制备金属镁,电解质溶液中镁离子不能放电不能得到金属镁,故D错误;
故选D.
B、过程②是加热氯化镁晶体失去结晶水得到固体氯化镁,镁离子在水溶液中会水解,结晶出的MgCl2?6H2O要在HCl氛围中加热脱水制得无水MgCl2,故B正确;
C、步骤③④是生成溴单质被还原剂吸收生成溴离子,加入氧化剂重新生成溴单质的过程,是富集溴元素的过程,故C正确;
D、电解熔融氯化镁制备金属镁,电解质溶液中镁离子不能放电不能得到金属镁,故D错误;
故选D.
点评:本题考查了海水资源应用,物质制备过程和工业流程的分析判断,主要是海水提取溴的原理应用,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一支25mL滴定管,内盛溶液液面在15.00mL刻度处,当将滴定管内液体全部排出时,所得液体的体积是( )
| A、10.00mL |
| B、15.00mL |
| C、小于10.00mL |
| D、大于10.00mL |
下列说法正确的是( )
| A、氧化还原反应的本质是反应前后有元素化合价的升降 |
| B、Ag++Cl-=AgCl↓ 的反应属于化合反应 |
| C、从1 L 1 mol/L的H2SO4溶液中取出10 mL该溶液,其中H+浓度为2 mol/L |
| D、晶体硅是制造光导纤维的原料 |
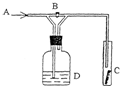 如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )
如图是一种试验氯气化学性质的实验装置,图中B为开关. 如先打开B,再让一种含氯气的气体从A处通入,C中干燥红色布条颜色褪色;当关闭B时,C处红色布条颜色无变化.则D瓶中盛有的溶液是( )①浓H2SO4②饱和NaCl溶液 ③浓NaOH溶液 ④饱和碳酸氢钠.
| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
下列物质:①NaCl ②HNO3 ③Cu(OH)2 ④NH3 ⑤AgNO3 ⑥H2O ⑦CH4 ⑧HClO
其中属于弱电解质的是( )
其中属于弱电解质的是( )
| A、②③⑥ | B、④⑤⑧ |
| C、③⑥⑧ | D、⑥⑧ |
酚醛树脂可用苯酚和甲醛反应制得.实验室制备酚醛树脂时,在酸性条件下,苯酚过量制得酚醛树脂若不易取出,则可趁热时加入一些乙醇来取出酚醛树脂;在碱性条件下,苯酚过量时,若酚醛树脂不易取出时,用加热或加溶剂的方法都很难将酚醛树脂取出.在上述两种情况下,下列有关叙述正确的是( )
| A、酸性条件制得的是体型结构酚醛树脂,碱性条件制得的是线型结构酚醛树脂 |
| B、酸性条件制得的是线型结构酚醛树脂,碱性条件制得的是网状结构酚醛树脂 |
| C、两种条件下制得的都是线型结构的酚醛树脂 |
| D、两种条件下制得的都是网状结构酚醛树脂 |
下列说法不正确的是( )
| A、Mg的金属性比Al强 |
| B、H2S的热稳定性比H2O强 |
| C、Na的原子半径比N原子大 |
| D、HClO4的酸性比H3PO4强 |