题目内容
7.下列有关金属的腐蚀与保护的说法正确的是( )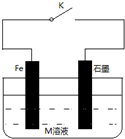
| A. | 常温下,关闭K时,若M溶液为浓硫酸,则石墨上有氢气放出 | |
| B. | 关闭K时,若M为氯化钠,则铁电极的电极反应式为:O2+4e-+2H2O═4OH- | |
| C. | 关闭K时,若M为则硫酸铵,则石墨极的电极反应式为:2H++2e-═H2↑ | |
| D. | 关闭K时,若M溶液为海水,石墨换成铜或银,则称为外加电流的阴极保护法 |
分析 A、常温下,关闭K时,若M溶液为浓硫酸,发生金属铁的析氢腐蚀;
B、关闭K时,若M为氯化钠,则发生金属铁的析氧腐蚀;
C、关闭K时,若M为则硫酸铵,显示酸性,发生金属铁的析氢腐蚀;
D、关闭K时,若M溶液为海水,石墨换成铜或银,此时金属铁是负极,会加快金属的腐蚀速率.
解答 A、常温下,关闭K时,若M溶液为浓硫酸,金属铁被钝化,石墨电极上不会产生氢气,故A错误;
B、关闭K时,若M为氯化钠,则发生金属铁的析氧腐蚀,金属铁是负极,铁电极的电极反应式为:Fe-2e-=Fe2+,故B错误;
C、关闭K时,若M为则硫酸铵,显示酸性,发生金属铁的析氢腐蚀,金属铁是负极,石墨极的电极反应式为:2H++2e-═H2↑,故C正确;
D、关闭K时,若M溶液为海水,石墨换成铜或银,此时金属铁是负极,会加快金属Fe的腐蚀速率,故D错误.
故选C.
点评 本题考查原电池原理,明确电极上发生的反应是解本题关键,注意金属的腐蚀和防护知识是关键,难度中等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
17.合金与纯金属制成的金属材料相比,合金的优点是( )
①合金的硬度一般比它的各成分金属的硬度大
②一般地,合金的熔点比它的各成分金属的熔点更低
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金
④合金比纯金属的导电性更强
⑤合金比纯金属的应用范围更广泛.
①合金的硬度一般比它的各成分金属的硬度大
②一般地,合金的熔点比它的各成分金属的熔点更低
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金
④合金比纯金属的导电性更强
⑤合金比纯金属的应用范围更广泛.
| A. | ①②③⑤ | B. | ②③④ | C. | ①②④ | D. | ①② |
18.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 乙醇、乙酸均能与Na反应放出氢气,二者分子中官能团相同 | |
| B. | 苯和油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体 | |
| D. | 纤维素和淀粉遇碘水均显蓝色 |
2.下列有关叙述正确的是( )
| A. | 所有酯类和糖类都可以发生水解反应 | |
| B. | 分馏石油得到的各个馏分都是混合物 | |
| C. | 棉花和蚕丝的主要成分都是纤维素 | |
| D. | 动物脂肪和植物油都属于酯类,都是高分子化合物 |
12.可在有机物中引入羟基的反应类型( )
①取代、②加成、③消去、④酯化、⑤氧化、⑥还原.
①取代、②加成、③消去、④酯化、⑤氧化、⑥还原.
| A. | ①②③ | B. | ①②⑤⑥ | C. | ①④⑤⑥ | D. | ①②③⑥ |
19.某固体中只可能含Cl-、SO42-、CO32-、Cu2+、Ba2+和Na+.探究小组为了确定该固体的组成,取该固体39g进行以下实验:(填写表中的空格)
(1)步骤二发生反应的离子方程式为2H++CO32-=CO2↑+H2O,步骤四发生反应的离子方程式为Ag++Cl-=AgCl↓.
(2)原固体中含有Na+的理由是溶液呈电中性,必须有阳离子,是否含有Cl-并说明理由碳酸钠与硫酸钠质量之和为39g,则不含氯离子.
| 实验操作与现象 | 实验结论 | |
| 步骤一 | 将该固体全部溶于于得无色溶液; | 肯定无Cu2+. |
| 步骤二 | 向上述溶液中加入足量盐酸,产生无色无味的气体共收集到2.24L(标准状况); | 肯定有CO32- 肯定无Ba2+ |
| 步骤三 | 向步骤二所得溶液中继续加入足量BaCl2溶液,产生沉淀,过滤并洗涤干燥后得46.6g白色沉淀. | 肯定有SO42- |
| 步骤四 | 向步骤三所得滤液中加入AgNO3溶液,得白色沉淀. |
(2)原固体中含有Na+的理由是溶液呈电中性,必须有阳离子,是否含有Cl-并说明理由碳酸钠与硫酸钠质量之和为39g,则不含氯离子.
16. 某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
 某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )
某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质,下列说法不正确的是( )| A. | 利用I、II装置制取气体(K2关闭、K1打开),可以收集H2等气体,但不能收集02、NO气体 | |
| B. | 利用II装置作简单改进(但不改变瓶口朝向)后,可以收集O2、NO等气体,但不能收集NO2气体 | |
| C. | 利用I、Ⅲ装置可以比较H2S04、H2CO3和H2SiO3的酸性强弱 | |
| D. | 利用I、Ⅲ装置既能验证氧化性:Ca(ClO)2>Cl2>Br2,又能保护环境 |
17. 利用微生物电池处理含乙酸钠和对氯酚
利用微生物电池处理含乙酸钠和对氯酚 的废水,工作原理如图所示.下列说法错误的是( )
的废水,工作原理如图所示.下列说法错误的是( )
 利用微生物电池处理含乙酸钠和对氯酚
利用微生物电池处理含乙酸钠和对氯酚 的废水,工作原理如图所示.下列说法错误的是( )
的废水,工作原理如图所示.下列说法错误的是( )| A. | 电极b是正极 | B. | 质子从b极移向a极 | ||
| C. | 处理后的废水pH降低 | D. | a极的电极反应式: +2e-+H+═ +2e-+H+═ +Cl- +Cl- |
