题目内容
14.某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源.已知制酒精的方法有三种:①在催化剂作用下乙烯与水反应②CH3CH2Br与氢氧化钠水溶液共热③(C6H10O5)n(淀粉)+nH2O→nC6H12O6(葡萄糖) C6H12O6(葡萄糖)→2C2H5OH+2CO2↑.
(1)方法①的化学反应方程式是CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.
(2)方法②的化学反应类型是取代反应(或水解反应).
(3)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?③,请简述理由:因为淀粉是可再生资源,而乙烯、溴乙烷都是来自于以石油为原料制得的产品,是不可再生资源.
(4)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是A
A.①B.③C.①③D.②③E.①②③
分析 (1)根据乙烯的性质分析,①为乙烯与水发生加成反应生成乙醇;
(2)②为卤代烃的水解反应;
(3)方法③中淀粉为可再生资源,而①中乙烯和②中溴乙烷都为石油为原料得到的产品,石油为不可再生资源;
(4)在有机反应中,加成反应原子利用率是100%,根据三种实验方案来回答.
解答 解:(1)加成反应的特点是“有去无回”和取代反应的特点是“有去有回”,乙烯和水之间发生的是加成反应,方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
(2)②为卤代烃的水解反应,反应CH3CH2Br+H2O$→_{△}^{NaOH}$CH3CH2OH+HBr中,溴原子被羟基取代,属于取代反应,
故答案为:取代反应(或水解反应);
(3)方法③中淀粉为可再生资源,而①中乙烯和②中溴乙烷都为石油为原料得到的产品,石油为不可再生资源,所以应该用方法③,
故答案为:③;因为淀粉是可再生资源,而乙烯、溴乙烷都是来自于以石油为原料制得的产品,是不可再生资源;
(4)加成反应原子利用率是100%,符合绿色化学的思想,①加成反应,②取代反应,③分解反应,故A正确,
故答案为:A.
点评 本题是一道化学和实际生产结合的题目,注意利用常见的有机化学反应类型及有机物的性质来解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.常温、常压下,50ml三种气态烃的混合物与足量的氧气混合后点燃爆炸,恢复到原来状况时,体积共缩小100ml,则三种烃可能是( )
| A. | CH4、C2H6、C3H4 | B. | C2H6、C3H6、C4H6 | C. | CH4、C2H6、C3H8 | D. | C2H4、C2H6、C2H2 |
2.下列实验合理的是( )
| A. | 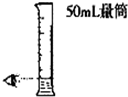 量取5.00ml盐酸 | |
| B. |  检验Fe2+离子 | |
| C. |  实验室制取氯气 | |
| D. | 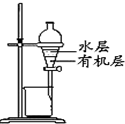 分离CCl4萃取碘水后的有机层和水层 |
9.原子序数为Z的元素在周期表中位于A、B、C、D四种元素的中间,则A、B、C、D四种元素的原子序数之和(如图所示)不正确的是(镧、锕系元素除外;且A、B、C、D中间再无其他元素)( )


| A. | 4Z | B. | 4Z+6 | C. | 4Z+10 | D. | 4Z+14 |
19.21世纪进入信息时代,两位美国化学家和一位日本化学家在导电塑料领域功勋卓著,他们首先把聚乙炔树脂制成导电塑料,开创塑料导电的新纪元.下列关于聚乙炔的叙述错误的是 ( )
| A. | 聚乙炔是以乙炔为单体发生加聚反应形成的高聚物 | |
| B. | 聚乙炔的化学式为 ,其分子中所有碳原子不可能在同一直线上 ,其分子中所有碳原子不可能在同一直线上 | |
| C. | 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质 | |
| D. | 1摩尔聚乙炔能与1摩尔Br2发生加成反应 |
6.有4种碳架如下的烃,下列说法中正确的是( )


| A. | b和c是同分异构体 | B. | a和d是同分异构体 | ||
| C. | a和d都能发生加成反应 | D. | 只有b和c能发生取代反应 |
4.组成和结构可用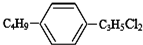 表示的有机物共有(不考虑立体结构)( )
表示的有机物共有(不考虑立体结构)( )
 表示的有机物共有(不考虑立体结构)( )
表示的有机物共有(不考虑立体结构)( )| A. | 36种 | B. | 32种 | C. | 27种 | D. | 18种 |