题目内容
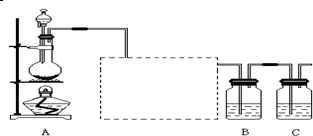
同温同压下,甲容器中所盛气体为CH4,乙容器中所盛气体为C2H2.
(1)若甲、乙两容器中所含氢原子数相等,则两容器所盛气体的体积之比为 .
(2)若甲、乙两容器中所含原子总数相等,则两容器所盛气体的物质的量之比为 .
(1)若甲、乙两容器中所含氢原子数相等,则两容器所盛气体的体积之比为
(2)若甲、乙两容器中所含原子总数相等,则两容器所盛气体的物质的量之比为
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
=
结合分子的组成计算;
(2)1molCH4含有5mol原子,1molC2H2含有4mol原子,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲、乙两容器中所含原子总数相等,则两容器所盛气体的物质的量之比为4:5.
| N |
| NA |
| V |
| Vm |
(2)1molCH4含有5mol原子,1molC2H2含有4mol原子,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲、乙两容器中所含原子总数相等,则两容器所盛气体的物质的量之比为4:5.
解答:
解:(1)由n=
=
可知,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲、乙两容器中所含氢原子数相等,两容器所盛气体的分子数之比为1:2,则两容器所盛气体的体积之比为1:2,
故答案为:1:2;
(2)1molCH4含有5mol原子,1molC2H2含有4mol原子,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲,乙两个容器所含原子总数相等,设甲、乙各为xmol和ymol,甲中原子数5xmol,乙中原子数4ymol,甲、乙两容器中所含原子总数相等,则 5x=4y,x:y=4:5,故答案为:4:5.
| N |
| NA |
| V |
| Vm |
故答案为:1:2;
(2)1molCH4含有5mol原子,1molC2H2含有4mol原子,同温同压下,气体的体积之比等于分子数之比等于物质的量之比,若甲,乙两个容器所含原子总数相等,设甲、乙各为xmol和ymol,甲中原子数5xmol,乙中原子数4ymol,甲、乙两容器中所含原子总数相等,则 5x=4y,x:y=4:5,故答案为:4:5.
点评:本题考查物质的量相关计算,题目难度不大,注意物质的量与体积、粒子数目的计算公式的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
钠在自然界中最主要的存在形式是( )
| A、金属钠 | B、硝酸钠 |
| C、硫酸钠 | D、氯化钠 |
下列水解离子方程式正确的是( )
| A、NH4++H2O?NH3?H2O+H+ |
| B、HCO3-+H2O?H3O++CO32- |
| C、CO32-+2H2O?H2CO3+2OH- |
| D、Fe3++3H2O?Fe(OH)3↓+3H+ |
“绿色商品”是指对环境无污染的商品,下列属于“绿色商品”的是( )
| A、含氟冰箱 | B、含铅汽油 |
| C、含磷洗涤剂 | D、含碘食盐 |