题目内容
下列离子方程式正确的是( )
| A、石灰水与过量碳酸氢钠溶液反应:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
| B、过量的CO2通入NaOH溶液中:CO2+OH-═HCO3- |
| C、硫酸铜与氢氧化钡溶液混合:Cu2++2OH-=Cu(OH)2 |
| D、氧化铜与稀硫酸反应:2H++O2-=H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.石灰水与过量碳酸氢钠溶液反应,生成碳酸钠、碳酸钙和和水;
B.过量的CO2通入NaOH溶液中,反应生成碳酸氢钠;
C.漏掉钡离子与氢氧根离子的反应;
D.氧化铜与稀硫酸反应生成硫酸铜和水.
B.过量的CO2通入NaOH溶液中,反应生成碳酸氢钠;
C.漏掉钡离子与氢氧根离子的反应;
D.氧化铜与稀硫酸反应生成硫酸铜和水.
解答:
解:A.石灰水与过量碳酸氢钠溶液反应,离子方程式:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-,故A正确;
B.过量的CO2通入NaOH溶液中,离子方程式:CO2+OH-═HCO3-,故B正确;
C.硫酸铜与氢氧化钡溶液混合,离子方程式:SO42-+Ba2++Cu2++2OH-=Cu(OH)2,↓+BaSO4↓,故C错误;
D.氧化铜与稀硫酸反应,离子方程式:2H++CuO=H2O+Cu2+,故D错误;
故选:AB.
B.过量的CO2通入NaOH溶液中,离子方程式:CO2+OH-═HCO3-,故B正确;
C.硫酸铜与氢氧化钡溶液混合,离子方程式:SO42-+Ba2++Cu2++2OH-=Cu(OH)2,↓+BaSO4↓,故C错误;
D.氧化铜与稀硫酸反应,离子方程式:2H++CuO=H2O+Cu2+,故D错误;
故选:AB.
点评:本题考查了离子方程式的书写,题目难度不大,熟悉反应的实质是解题关键,注意化学式的拆分、反应物用量对反应的影响.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,2.8g N2与C2H4的混合气体所含电子数为1.4 NA |
| B、标准状况下,1.12LNO与1.12O2的混合物中含有的原子数为0.2NA |
| C、Na2O2与H2O反应生成1.12LO2(标准状况),反应中转移的电子数为0.2NA |
D、32gS8单质中含有的S-S键个数为2NA |
可用H++OH-═H2O表示的化学反应是:( )
①H2SO4+Ba(OH)2
②HNO3+Fe(OH)3
③KHCO3+KOH
④HCl+NaOH
⑤CH3COOH+KOH
⑥NaHSO4+KOH.
①H2SO4+Ba(OH)2
②HNO3+Fe(OH)3
③KHCO3+KOH
④HCl+NaOH
⑤CH3COOH+KOH
⑥NaHSO4+KOH.
| A、全部 | B、①③④⑥ |
| C、②④⑤ | D、④⑥ |
下列离子方程式的书写正确的是( )
| A、铝与盐酸反应:Al+6H+═Al3++3H2↑ |
| B、少量CO2通入Ca(OH)2溶液中:CO2+2OH-═CO32-+H2O |
| C、氢氧化钠溶液与盐酸反应:NaOH+H+═H2O+Na+ |
| D、碳酸钠与氯化钙混合:CO32-+Ca2+═CaCO3↓ |
下列分散系中分散质粒子最大的是( )
| A、蔗糖溶液 |
| B、少量植物油和水的混合物 |
| C、牛奶 |
| D、硫酸溶液 |
下列离子方程式与所述事实相符且正确的是( )
| A、用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
| B、用双氧水和稀硫酸可以雕刻印刷电路板:Cu+H2O2+2H+=Cu++2H2O |
| C、KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=2H2O+I2 |
| D、澄清石灰水与过量苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O. |
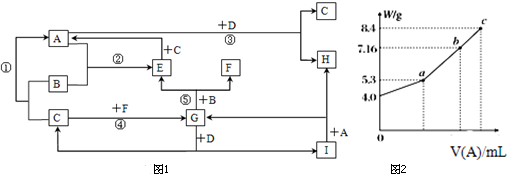
 使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量w和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的质量之比为( )
使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量w和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的质量之比为( )| A、2:3 | B、1:1 |
| C、4:3 | D、8:9 |